- 偏铝酸钾

偏铝酸钾
基本信息
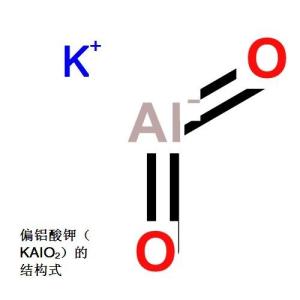 偏铝酸钾的结构式【中文名】偏铝酸钾
偏铝酸钾的结构式【中文名】偏铝酸钾
【英文】potassium metaaluminate
【化学式】KAlO2
【溶解性】 可溶于水
【相对分子质量】大约为98
【状态】 常温下为白色固体[1]
生成
1、与偏铝酸钠的生成类似,偏铝酸钾可由铝、氢氧化铝或氧化铝与氢氧化钾溶液反应生成
2Al+2KOH+2H2O=2KAlO2+3H2↑
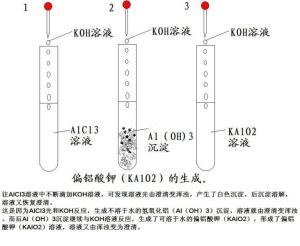 偏铝酸钾的生成Al(OH)3+KOH=KAlO2+2H2OAl2O3+2KOH=2KAlO2+H2O
偏铝酸钾的生成Al(OH)3+KOH=KAlO2+2H2OAl2O3+2KOH=2KAlO2+H2O
2、偏铝酸钾还可以由铝盐加过量氢氧化钾生成
AlCl3+4KOH=KAlO2+3KCl+2H2O[1]
化学性质
概述
由于偏铝酸钾和偏铝酸钠都含有偏铝酸根离子,故而,偏铝酸钾的很多化学性质与偏铝酸钠类似,比如与强酸反应,和二氧化碳反应,与铝离子反应。其中,参与这些反应的是偏铝酸根离子,钾离子不参加反应。
而因为偏铝酸根是弱酸根,所以偏铝酸根会水解,故而偏铝酸钾溶液呈碱性。
另外,偏铝酸钾还可以与浓硫酸反应,生成明矾(十二水合硫酸铝钾)。[2]
强酸反应
偏铝酸钾溶液可以与强酸(比如盐酸等)反应,生成氢氧化铝,如果强酸过量,还可生成铝离子
KAlO2+HCl+H2O=Al(OH)3↓+KCl
KAlO2+4HCl=AlCl3+2H2O+KCl[2]
二氧化碳反应
偏铝酸钾溶液与二氧化碳发生反应,生成碳酸钾和氢氧化铝。但是,氢氧化铝并不和二氧化碳反应,但碳酸钾会和二氧化碳继续反应,生成碳酸氢钾。故而,在二氧化碳适量时,生成的是氢氧化铝和碳酸钾,二氧化碳过量时,生成氢氧化铝和碳酸氢钾
2KAlO2+CO2+3H2O=2Al(OH)3↓+K2CO3(二氧化碳适量)
KAlO2+CO2+2H2O=Al(OH)3+KHCO3(二氧化碳过量)
铝离子反应
偏铝酸钾会和铝离子发生双水解反应,生成氢氧化铝
AlCl3+3KAlO2+6H2O=4Al(OH)3↓+3KCl[2]
碳酸氢根离子
偏铝酸钾不仅仅会和铝离子反应,和碳酸氢根离子也会发生类似强酸制弱酸的反应(碳酸氢根将它的氢给偏铝酸根,自己形成碳酸根,这是一个单方给予的过程;而双水解则是一个从水那里各取所需的过程),二者在溶液中不能共存。比如偏铝酸钾会和碳酸氢钾发生化学反应,生成碳酸钾和氢氧化铝。偏铝酸钾和碳酸氢钾的反应方程式为:
KAlO2+KHCO3+H2O=Al(OH)3↓+K2CO3
由于钾离子实际上并不参加反应,参加反应的是偏铝酸根离子,故而,该反应化为离子方程式为: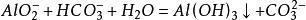
证明:因为碳酸的二级电离常数为:
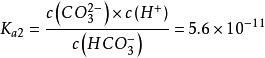
而氢氧化铝的酸式溶度积常数为:
![]()
而由于偏铝酸钾和碳酸氢盐(如碳酸氢钾)反应的化学平衡常数为
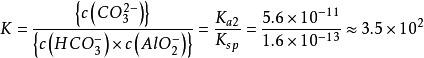
常数较大,反应显然能发生。
同理,偏铝酸钾还会和亚硫酸钾、磷酸二氢钾反应,故而偏铝酸钾与碳酸氢盐(如碳酸氢钾(KHCO3))、亚硫酸氢盐溶液(如亚硫酸氢钾(KHSO3))、磷酸二氢盐溶液(如磷酸二氢钾(KH2PO4))都不能共存于同一溶液中。但是,偏铝酸钾可以和碳酸根共存于同一溶液中。[2]
生成明矾
在偏铝酸钾溶液中加入过量浓硫酸,可生成溶解度较小的复盐明矾(KAl(SO4)2·12H2O)。反应式为:
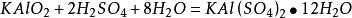
故该反应可用于制备明矾。
水解
由于偏铝酸钾中的偏铝酸根是弱酸根离子,故而偏铝酸钾可在水中发生水解,参与水解的是偏铝酸根离子,钾离子并不参加反应。
由于偏铝酸根离子水解的缘故,偏铝酸钾溶液呈碱性。反应方程式为(注:该反应可逆):
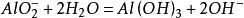
反应实质
在关于偏铝酸钾的很多反应中,由于钾离子不参与反应,故而参与反应的实际上是偏铝酸根离子。
与强酸发生反应: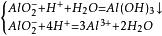 (注:上面的反应是酸适量时发生,下面的反应是酸过量时发生)
(注:上面的反应是酸适量时发生,下面的反应是酸过量时发生)
与弱酸H2CO3发生反应,即通入CO2气:
∵Al(OH)3酸性<H2CO3,且Al(OH)3酸性<![]()
∴反应为: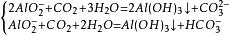 (注:上面的反应是CO2适量时发生,下面的反应是CO2过量时发生)
(注:上面的反应是CO2适量时发生,下面的反应是CO2过量时发生)
与铝离子反应:铝盐和偏铝酸盐溶液互促水解反应
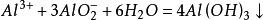
旧认识更正
 偏铝酸钾人教版教材中编写道:氢氧化铝溶于氢氧化钠溶液生成偏铝酸钠溶液,而后来的山东科学技术出版社出版的化学教材(必修一)中,讲到铝和其金属材料一课中,说Al和NaOH和水反应生成Na[Al(OH)₄]四羟基合铝酸钠。这是怎么一回事呢?实际上,偏铝酸钠在水溶液中都是以Na[Al(OH)₄]的形式存在,以前只不过是为了方便,把它简写成NaAlO₂。但它的实际组成还是Na[Al(OH)₄]。
偏铝酸钾人教版教材中编写道:氢氧化铝溶于氢氧化钠溶液生成偏铝酸钠溶液,而后来的山东科学技术出版社出版的化学教材(必修一)中,讲到铝和其金属材料一课中,说Al和NaOH和水反应生成Na[Al(OH)₄]四羟基合铝酸钠。这是怎么一回事呢?实际上,偏铝酸钠在水溶液中都是以Na[Al(OH)₄]的形式存在,以前只不过是为了方便,把它简写成NaAlO₂。但它的实际组成还是Na[Al(OH)₄]。
不仅仅是偏铝酸钠,偏铝酸钾等其它偏铝酸盐也类似。偏铝酸根在水溶液中是以四羟基合铝酸根的形式存在,只不过为了方便,才把它写成偏铝酸根的形式,但偏铝酸盐的实际组成仍是四羟基合铝酸根。
因此,根据上述结论,偏铝酸钾在水溶液中也是以四羟基合铝酸钾(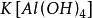 )的形式存在,为了书写方便,故而把四羟基合铝酸钾仍旧写成了偏铝酸钾(KAlO2),但偏铝酸钾在溶液中的实际组成仍然是四羟基合铝酸钾。真正的偏铝酸钾只能在熔融状态下存在。[2]
)的形式存在,为了书写方便,故而把四羟基合铝酸钾仍旧写成了偏铝酸钾(KAlO2),但偏铝酸钾在溶液中的实际组成仍然是四羟基合铝酸钾。真正的偏铝酸钾只能在熔融状态下存在。[2]

-
中国铝业集团有限公司
2025-09-24 05:58:34 查看详情 -
18款奥迪A6L车门材质是铝合金的吗
2025-09-24 05:58:34 查看详情


 求购
求购







