- 地夫可特

地夫可特
基本资料
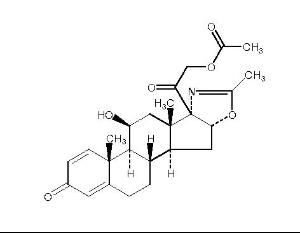 地夫可特
地夫可特
中文别名:地恶唑可特、地拉扎可、去氟可特
英文名称:deflazacort
英文别名:azacort、deflan、deflazacortum、flantadin、lantadin、oxazacort
CAS编号:14484 -47-0
分子式:c25h31no6
分子量:441.52
含量:99%
性 状:白色或类白色结晶粉末
用 途:具有抗炎、抗过敏作用,相当于泼尼松龙的10-20倍,用于肾上腺皮质机能减退、自身免疫性疾病、过敏性疾病及血液系统疾病等。
物理性质
 英文别名:11b,21-Dihydroxy-2'-methyl-5'bH-pregna-1,4-dieno[17,16-d]oxazole-3,20-dione 21-acetate;DEFLAZACORT INTERMEDIATE;(4AR,4BS,5S,6AS,9AR,10AS,10BS)-6B-ACETYL-5-HYDROXY-4A,6A,8-TRIMETHYL-4A,4B,5,6,6A,6B,9A,10,10A,10B,11,12-DODECAHYDRO-9-OXA-7-AZA-PENTALENO[2,1-A]PHENANTHREN-2-ONE;2-(5-hydroxy-4a,6a,8-trimethyl-2-oxo-2,4a,4b,5,6,6a,9a,10,10a,10b,11,12-dodecahydro-6bH-naphtho[2',1':4,5]indeno[1,2-d][1,3]oxazol-6b-yl)-2-oxoethyl acetate;2-[(4aR,4bS,5S,6aS,6bS,9aR,10aS,10bS)-5-hydroxy-4a,6a,8-trimethyl-2-oxo-2,4a,4b,5,6,6a,9a,10,10a,10b,11,12-dodecahydro-6bH-naphtho[2',1':4,5]indeno[1,2-d][1,3]oxazol-6b-yl]-2-oxoethyl acetate;(4aR,4bS,5S,6aS,9aR,10aS,10bS)-6b-acetyl-5-hydroxy-4a,6a,8-trimethyl-4a,4b,5,6,6a,6b,9a,10,10a,10b,11,12-dodecahydro-2H-naphtho[2',1':4,5]indeno[1,2-d][1,3]oxazol-2-one;
英文别名:11b,21-Dihydroxy-2'-methyl-5'bH-pregna-1,4-dieno[17,16-d]oxazole-3,20-dione 21-acetate;DEFLAZACORT INTERMEDIATE;(4AR,4BS,5S,6AS,9AR,10AS,10BS)-6B-ACETYL-5-HYDROXY-4A,6A,8-TRIMETHYL-4A,4B,5,6,6A,6B,9A,10,10A,10B,11,12-DODECAHYDRO-9-OXA-7-AZA-PENTALENO[2,1-A]PHENANTHREN-2-ONE;2-(5-hydroxy-4a,6a,8-trimethyl-2-oxo-2,4a,4b,5,6,6a,9a,10,10a,10b,11,12-dodecahydro-6bH-naphtho[2',1':4,5]indeno[1,2-d][1,3]oxazol-6b-yl)-2-oxoethyl acetate;2-[(4aR,4bS,5S,6aS,6bS,9aR,10aS,10bS)-5-hydroxy-4a,6a,8-trimethyl-2-oxo-2,4a,4b,5,6,6a,9a,10,10a,10b,11,12-dodecahydro-6bH-naphtho[2',1':4,5]indeno[1,2-d][1,3]oxazol-6b-yl]-2-oxoethyl acetate;(4aR,4bS,5S,6aS,9aR,10aS,10bS)-6b-acetyl-5-hydroxy-4a,6a,8-trimethyl-4a,4b,5,6,6a,6b,9a,10,10a,10b,11,12-dodecahydro-2H-naphtho[2',1':4,5]indeno[1,2-d][1,3]oxazol-2-one;
EINECS号:238-483-7
分子式:C23H29NO4
分子量:383.48
InChI:InChI=1/C23H29NO4/c1-12(25)23-19(28-13(2)24-23)10-17-16-6-5-14-9-15(26)7-8-21(14,3)20(16)18(27)11-22(17,23)4/h7-9,16-20,27H,5-6,10-11H2,1-4H3/t16-,17-,18-,19+,20+,21-,22-,23?/m0/s1
沸点:544.2°C at 760 mmHg
闪点:282.9°C
外观性状,白色或类白色结晶粉末
用途:皮质甾类医药原料及中间体
应用
1 功用作用: 具有抗炎、抗过敏作用,相当于泼尼松龙10~20倍,用于肾上腺皮质机能减退、自身免疫性疾病、过敏性疾病及血液系统疾病等
2 用法与用量:口服,每日6~60mg,可增至90mg。
3 禁用慎用:
3.1 一般性的感染不应使用本药。对病毒性感染应慎用,以免因抑制机体免疫系统功能而导致病毒感染的扩散与加重。
3.2 孕妇应慎用或禁用。肝功能不良病人不宜用。
3.3 高血压、糖尿病、肾上腺皮质机能亢进症、活动性溃疡及新近胃肠吻合手术、心力衰竭、精神病、癫痫、动脉硬化、血栓性静脉炎、骨质疏松、耐药性感染及真菌感染等慎用或禁用。
4 给药说明:
4.1 应用本类药物时,必须严格掌握适应症,防止滥用,以减少不良反应和并发症。用药期间应测定肾功能。
4.2 治疗急性感染中毒,必须与足量的抗感染药物配合应用。
4.3 长期使用本品时,应给予促皮质素。医学教育网搜集整理
4.4 停药时应逐渐减量,不可骤停,以免复发或出现肾上腺皮质机能不足症状。
4.5 已经长期使用本品的病人,在手术时及术后的3-4天内,须适当增加用量,以防止皮质功能不足,一般外科病人尽量不用,以免影响伤口愈合。
4.6 密闭置干燥阴凉处保存。
5 不良反应:
5.1 本品在大剂量长期应用时,可引起肥胖、多毛、痤疮、血糖升高、高血压、眼内压升高、钠和水储留、水肿、血钾降低、精神兴奋、胃及十二指肠溃疡甚至出血穿孔、骨质疏松、脱钙、病理性骨折、伤口愈合不良、柯兴氏综合症等。
5.2 本品对病原微生物并无抑制作用,且由于能抑制炎症反应和免疫反应,降低机体的防御功能,反而有可能使潜在的感染病灶活动并扩散,应特别注意及时加以控制。特别是因缺乏具有确切疗效的抗病毒药物,病毒性感染病人用药可能会导致不能控制的病毒感染扩散与加重。
5.3 长期使用本品可能导致肾上腺皮质功能减退,可加用促皮质素。
5.4 妊娠期间特别是早期使用可能会影响胎儿的发育,甚至造成多发性畸形。
地夫可特合成
地夫可特 【药效类别】肾上腺皮质激素类药【分 子 式】C25H31NO6 【分 子 量】441.52 收录药典】 【收录药典】JP14 开发单位】 (意大利 意大利) 【开发单位】Gruppo Lepetit S.P.A (意大利) 首次上市】 【首次上市】1985 年,意大利 结晶。 溶于丙酮等极性有机溶剂。 Mp156.5℃ [α]D+62.5℃(C=0.5, +62.5℃(C=0.5, 【性 状】 结晶。 溶于丙酮等极性有机溶剂。 Mp156.5℃。 CHCl3)。 【用 途】 甾体抗炎药。为第三代糖皮质激素具有消炎、抗过敏增加糖原异生等作用。 甾体抗炎药。为第三代糖皮质激素具有消炎、抗过敏增加糖原异生等作用。 作用相当于泼尼龙的 10~20 倍,氢化可的松的 40 倍。用于治疗原发及继发性肾 上腺皮质功能减退、风湿病胶原性疾病、皮肤病、变应性疾病、眼科疾病、 上腺皮质功能减退、风湿病胶原性疾病、皮肤病、变应性疾病、眼科疾病、暴 发性和播散性肺结核、造血系统疾患、溃疡性结肠炎、特发性肾病综合征, 发性和播散性肺结核、造血系统疾患、溃疡性结肠炎、特发性肾病综合征,造 血系统恶性肿瘤等症。 血系统恶性肿瘤等症。 一、17α-溴-3β,16β-二羟基-5α-孕甾-11,20-二酮-3-乙酸酯(2)的制备 在反应瓶中,加入 3β-羟基-5α-孕甾-16-烯-11,20-二酮-3-乙酸酯 175g (0.47mol)和四氢呋喃 2.3L,冰浴冷却至 10℃,于搅拌下加入 0.46mol/L 高氯酸 溶液 1.34L 和 N-溴乙酰胺 1.153g(8.35mol),加毕,避光搅拌 4h。反应毕,反 应液用饱和亚硫酸钠溶液洗至无色,减压浓缩,冷却,析出固体,水洗,于 40℃ 下真空干燥, 得粗品(2)229.2g, mp169~172℃。 用苯重结晶, 得(2), mp169~172℃。 1 IR(KBr): ν3500(-OH); 1720, 1700, (C=0) 1250, 1690 , 1025cm-1。 H-NMR: δ8.95(s, 3H,C18-H),8.88(s,3H,C19-H),7.97(s,3H,CH3COO),7.85(s,2H,C21-H) 二、16β,17β-环氧-3-羟基-5α,17α-孕甾-11,20-二酮(3)的制备 1 在反应瓶中,加入(2)222g(0.473mol)、甲醇 2.0L,加热升温至回流,于搅 拌下加入含氢氧化钾 73g(1.30mol)的 80%甲醇-水混合溶液 546ml,继续加热搅 拌回流 50min。反应毕,减压回收溶剂,得粗品(3)170g。mp172~175℃。用苯重 结晶,得(3)。mp177~178℃。[α]D=+11.3°(苯)。IR (KBr):ν3650(-OH); 1710(C=0);1033cm 。 H-NMR (CDCl3):δ9.20(s,3H,C18-H);9.02(s,3H, C19-H);8.00(s,3H,C21-H)。 三、17α-叠氮-3β,16α-二羟基-5α-孕甾-11,20-二酮(4)的制备 在干燥反应瓶中,加入(3)82g(0.237mol),叠氮钠 246g(3.785mol),二甲 基亚砜 1.23L 和 98%硫酸 16.9ml(0.317mol), 92~94℃搅拌 105min。 于 反应毕, 将反应液立即倒入已预冷至 0℃的 5%盐酸溶液 8.0L 中,析出固体,过滤;将固 体溶于适量二氯甲烷中,依次用稀盐酸,5%碳酸钠溶液和水洗涤,无水硫酸钠干 燥。过滤,滤液回收溶剂,析出固体,将固体溶于 5%丙酮的氯仿溶液,硅胶 180g 纯化[洗脱剂:丙酮-三氯甲烷(5:95)],收集所需组分,减压浓缩,得(4)18.2g。 用甲醇重结晶,得(4)。mp233~234℃。[α]D=-48.3°(C=0.5,CH3OH)。IR (KBr): ν3650(OH),2125(N=N=N) 1700(C=0),1030cm-1。1H-NMR (CDCl3):δ9.41(s, 3H,C18-H);9.01(s,3H,C19-H);7.73(s,3H,C21-H)。 四、3β,16α-二乙酰氧基-17α-叠氮-5α-孕甾-11,20-二酮(5)的制备 在干燥反应瓶中,加入(4)38.95g(0.l0mol),乙酸酐 51.0g(0.50mol),吡 啶 23.73g(0.30mol), 加热搅拌回流 15h。 反应毕, 减压浓缩至干, 得(5)粗品(可 直接用于下步反应)。mp167~169℃,[α]D=-82.4°,IR (KBr):ν2125(N=N=N), 1720~1740(C=O 酯基),1710(C=O 甾环),1240~1026cm-1。1H-NMR:δ9.60(s, 3H,C18-H);9.02(s,3H,C19-H);7.95~8.02(s,6H,2xCH3COO);7.76(s,3H, C21-H)。 五、 3β-乙酰氧基-5α-孕甾-11,20-二酮[17α,16α-d]-2'-甲基恶唑啉(6) 的制备 在反应瓶中,加入(5)72.0g(0.152mol)、氧化铂 5g(0.024mol)、甲醇 3.1L, 于常温常压通氢氢化 2.5h。反应毕,过滤,回收催化剂。滤液减压回收溶剂至 干,得(6) (备用)。 六、3β-羟基-5α-孕甾-11,20-二酮[17α,16α-d]-2'一甲基恶唑啉(7)的 -1 1 2 制备 在反应瓶中,加入上步所得(6)和 10%盐酸 250ml,加热搅拌回流 15min。反 应毕,冷却,得清澈溶液,加入 10%氢氧化钠溶液至固体析出完全。过滤,干燥, 得(7)58g (98.5%),mp210~212℃。 七、3β-羟基-5α-孕甾-11,20-二酮[17α,16α-d]-2'-甲基恶唑啉-20-酮 缩胺基脲(8)的制备 在反应瓶中,加入(7)10g(0.0258mol)、甲醇 350ml,加热搅拌回流,立即 加入盐酸氨基脲 8.3g(0.0744mol)、吡啶 5.75ml 和水 50ml 的溶液,继续加热搅 拌回流 5h。反应毕,减压浓缩至干。剩余物中加入水 300ml,析出固体,过滤, 干燥,得(8)11.5g(100%),mp255~258℃,IR (Nujol):ν3450(OH),1690,1655, 1575cm-1。1H-NMR (C5D5N):δ9.26(s,3H,C18-H):8.87(s,3H,C19-H);7.93(s, 3H,C21-H);7.73(s,3H,C2'-CH3)。 八、3β,11β-二羟基-5α-孕甾-20-酮[17α,16α-d]-2'-甲基恶唑啉-20酮缩氨基脲(9)的制备 在反应瓶中,加入(8)9.0g(0.02mol)、95%乙醇 230ml,在氮气保护下,依 次加入预热至 65℃的含碳酸氢钾 3.6g 的 36ml 溶液和粉末状硼氢化钠 2.34g(0.062mol),于搅拌下加热回流 0.5h,加入粉末状硼氢化钠 2.34g(0.062mol),于搅拌下加热回流 0.5h,加入粉末状硼氢化钠 2.34g(0.062mol),继续搅拌加热回流 1.5h。反应毕,冷却,用 5%乙酸调至溶液 pH7,减压浓缩至剩余液约 200ml。剩余物中,加入适量水,冷却,析出固体, 过滤,干燥,得(9)8.5g(94%),mp277~281℃。IR (Nujol):ν3300 (OH 和 NH), -1 1 1680,1655,1575cm 。 H-NMR (C5D5N):δ8.73(s,3H,C18-H):8.67(s,3H, C19-H);7.97(s,3H,C21-H );7.68ppm(s,3H,2'-CH3)。 九、3β,11β-二羟基-5α-孕甾-20-酮[17α,16α-d]-2'-甲基恶唑啉(10) 的制备 在反应瓶中,加入(9)7.7g(0.0172mol)、甲醇 75ml 和 10%盐酸 75ml,加热 搅拌回流 1h。反应毕,稍冷,加入适量活性炭脱色,过滤,滤液减压回收溶剂, 剩余物,加入 10%氢氧化钠至完全析出固体,过滤,干燥,得粗品 (10)6.3g(93.8%)。Mp240~250℃。用甲醇重结晶,得(10),mp255~258℃。 3 [α]D=+103.8°(C=0.5,二氧六环)。 IR (Nujol):ν3380 和 3280(OH), 1700(C20=0),1640(C=N)cm 。 H-NMR (C5D5N):δ8.79(s,3H,C18-H);8.68(s, 3H,C19-H);7.99 和 7.67ppm(C21-H 和 CH3C=N)。 十、11β-羟基-5α-孕甾-3,20-二酮[17α,16α-d]-2'-甲基恶唑啉(11)的 制备 在干燥反应瓶中, 加入(10)12.5g(0.032mol), 无水甲苯 500ml, 环己酮 90ml 和异丙醇铝 6.24g(0.0305mol),加热搅拌回流 2h。反应毕,减压回收溶剂至干, 剩余物用甲醇提取数次,合并有机层,减压浓缩,剩余物经硅胶柱[洗脱剂:三 氯甲烷]纯化,收集所需组份,减压浓缩至干,得(11)9.0g(75%),mp196~200℃, [α]D=+108°(C=0.5,CHCl3)。1H-NMR(CDCl3):δ9.08(s,3H,C18-H);8.72(8, 3H,C19-H),8.01 和 7.73(C21-H 和 2'-CH3) 十一、 2,4-二溴-11β-羟基-5α-孕甾-3,20-二酮[17α,16α-d]-2'-甲基恶 唑啉(12)的制备 在干燥反应瓶中,加入(11)6.5g(0.0168mol),无水二氧六环 123ml 和 25% 溴化氢乙酸溶液 8.2ml,于搅拌下,滴加溴素 5.5g(0.0344mol)和二氧六环 50ml 的溶液, 1h 滴毕, 约 于室温继续搅拌 0.5h。 反应毕, 将反应液倒入含乙酸钾 35.0g 的冷水 1.0L 中,析出固体,过滤,干燥,得(12)(直接用于下步反应)。 十二、3β-羟基-孕甾-1,4-二烯-3,20-二酮[17α,16α-d]-2'-甲基恶唑啉 (13)的制备 在反应瓶中,加入上步所得(12)和 N,N-二甲基甲酰胺 120ml,在氮气保护 下,加入溴化锂 2.88g(0.0275mol),碳酸锂 5.76g,于 140℃搅拌 4h。反应毕, 加入适量水,用乙酸乙酯提取数次,合并有机层,无水硫酸钠干燥,过滤。滤液 回收溶剂,剩余物经硅胶柱[洗脱剂:苯-三氯甲烷-乙醇]纯化,收集所需组分, 减压浓缩, 得(13)5.1g(80%), mp275~280℃。 用甲醇重结晶, 得(13), mp279~280℃。 [α]D=+103.3° (C=0.5, CHCl3) UV(CH3OH): λmax 240~242nm。 。 IR(KBr): ν3400 1 和 3600 (OH) 1738 21=O) 1720(C20=O), , (C , 1650(C3=O, C=N)cm-l。 H-NMR(CDCl3): -1 1 δ9.02(s,3H,C18-H);8.52(s,3H,C19-H);8.06 和 7.75ppm(C21-H 和 2'-CH3)。 十三、 11β-羟基-21-碘-孕甾-1,4-二烯-3,20-二酮[17α,16α-d]-2'-甲基 恶唑啉(14)的制备 4 在反应瓶中,加入(13)20g(5.2mol)、四氢呋喃-甲醇(1:1)溶液 100ml、氧 化钙 3g(0.0536mol)和 α,α-偶氮二异丁腈 0.1g,于剧烈搅拌下滴加腆 2.0g(7.87mmol)和四氢呋喃-甲醇(1:1)的溶液, 继续搅拌至溶液无色为止。 过滤, 滤液依次用冷的 3.0%硫代硫酸钠溶液和水洗涤,有机层减压浓缩至干,析出固 体,得(14)。mp226~228℃。 十四、地夫可特(1)的合成 在反应瓶中,加入上步所得(14)和丙酮 50ml,搅拌溶解,加入三乙胺 20ml、 冰乙酸 12ml,加热搅拌回流 1h。反应毕,加入适量水,分出有机层,减压浓缩 至干,剩余物经硅胶柱[洗脱剂:苯-三氯甲烷-乙醇(49:49:2)]纯化,收集所需 组份, 浓缩至干, 得粗品(1)固体。 用丙酮-己烷重结晶, 得(1)1.6g(70%) (系(14) 至(1)两步连乘的收率),mp256.5℃。 【光谱数据】 [2] UV(CH3OH):λmax 241~243 nm。 IR(KBr): ν3600 和 3400(OH), 1738(C21=0), 1720(C20=0), 1650(C3=0, C=N), 886cm-1。 1 H-NMR (CDCl3):δ8.97(s,3H,C18-H);8.56(s,3H,C19-H);8.05 和 7.92 (CH3COO 和 CH3C=N-)

-
江铃福特轻客持续打造最优TCO 江铃特顺柴油版怎么样
2025-09-20 14:45:02 查看详情 -
江铃福特领界怎么样 江铃特顺轻客怎么样
2025-09-20 14:45:02 查看详情 -
格拉伦·布莱恩特·班克斯
2025-09-20 14:45:02 查看详情 -
厦门市特房筼筜开发有限公司
2025-09-20 14:45:02 查看详情 -
T70对比江铃域虎7 江铃特顺柴油版怎么样
2025-09-20 14:45:02 查看详情 -
江铃福特领睿购车手册 江铃特顺轻客怎么样
2025-09-20 14:45:02 查看详情


 求购
求购






