- 硫化物

硫化物
硫化物的定义
 插件(4)-2价硫的化合物,金属硫化物可以看成氢硫酸的盐。金属与硫直接反应或者将硫化氢气体通入金属盐溶液,或者往盐溶液中加入硫化钠,都可制得金属硫化物。
插件(4)-2价硫的化合物,金属硫化物可以看成氢硫酸的盐。金属与硫直接反应或者将硫化氢气体通入金属盐溶液,或者往盐溶液中加入硫化钠,都可制得金属硫化物。
碱金属硫化物和硫化铵易溶于水,由于水解其溶液显碱性。碱土金属、钪、钇和镧系元素的硫化物较为难溶。当阳离子的外层电子构型为18电子和18+2电子时,往往由于较强的极化作用而形成难溶的、有颜色的硫化物。大多数不溶于水的硫化物可溶于酸并释放出硫化氢,极难溶的少数金属硫化物(如CuS、HgS)可用氧化性酸将其溶解,此时S被氧化成硫而从溶液中析出。难溶金属硫化物在溶液中存在溶解-沉淀平衡。控制溶液的酸度,可以改变溶液中S[1]
硫化物合成
无机硫化物通常可通过以下方法合成:(注:K为国际温度单位开尔文)
1、单质直接化合,例如:
C + 2S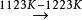 CS2
CS2
2、硫酸盐或高价硫化物的还原,例如:
Na2SO4+ 4C→ Na2S + 4CO 1373K
In2S3+ 2![]() → In2S + 2H2S
→ In2S + 2H2S
3、溶液中或高温的复分解反应,例如:
FeCl2+ H2S → FeS↓ + 2HCl
3SiO2+ 2Al2S3→ 3SiS2+ 2Al2O3 1373K
4、以硫代酸盐为原料制取,例如:
(NH4)2MoO4+ 4(NH4)2S + 4H2O → (NH4)2[MoS4] + 8NH3·H2O
(NH4)2MoO4+ 2HCl --(加热)→ MoS3+ H2S + 2NH4Cl
5、高价硫化物加热分解,例如:
MoS3--(加热)→ MoS2+ S[1]
物理性质
颜色
| 几种硫化物的颜色 | |||||||
|---|---|---|---|---|---|---|---|
| Al2S3 | 黄 | GeS | 灰黑 | P4S5 | 亮黄 | CdS | 黄 |
| Ga2S3 | 黄 | SnS2 | 黄 | P4S10 | 黄 | HgS | 红/黑 |
| In2S3 | 黄/红 | SnS | 棕黑 | As4S4 | 红 | MnS | 绿/肉 |
| InS | 酒红 | PbS | 黑 | As4S6 | 黄 | MoS3 | 红棕 |
| Tl2S3 | 蓝黑 | As4S10 | 淡黄 | RuS2 | 灰蓝 | ||
| Tl2S | 黑 | Sb2S3 | 橙红 | FeS2 | 黄 | ||
| Bi2S3 | 棕黑 | ||||||
硫化物大多含有鲜艳的颜色,见上表。 除此之外,MoS2、Re2S7、FeS、CoS2、NiS、PtS2、Cu2S、CuS和Ag2S等过渡金属硫化物都是黑色的。
溶解性
| 几种硫化物的颜色 | |||||||
|---|---|---|---|---|---|---|---|
| Al2S3 | 黄 | GeS | 灰黑 | P4S5 | 亮黄 | CdS | 黄 |
| Ga2S3 | 黄 | SnS2 | 黄 | P4S10 | 黄 | HgS | 红/黑 |
| In2S3 | 黄/红 | SnS | 棕黑 | As4S4 | 红 | MnS | 绿/肉 |
| InS | 酒红 | PbS | 黑 | As4S6 | 黄 | MoS3 | 红棕 |
| Tl2S3 | 蓝黑 | As4S10 | 淡黄 | RuS2 | 灰蓝 | ||
| Tl2S | 黑 | Sb2S3 | 橙红 | FeS2 | 黄 | ||
| Bi2S3 | 棕黑 | ||||||
化学性质
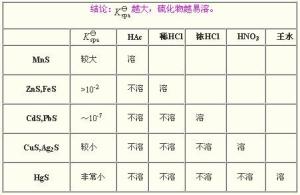 金属硫化物在酸中溶解性金属的酸式硫化物都可溶于水,但正盐中只有碱金属硫化物和硫化铵可溶。一般地讲,金属硫化物的溶解度可通过阳离子极化力(离子电荷数/离子半径,Z/r)的大小来预测。阳离子极化能力的增强,将导致化合物共价性的增加,极性减小,因而溶解度也降低。
金属硫化物在酸中溶解性金属的酸式硫化物都可溶于水,但正盐中只有碱金属硫化物和硫化铵可溶。一般地讲,金属硫化物的溶解度可通过阳离子极化力(离子电荷数/离子半径,Z/r)的大小来预测。阳离子极化能力的增强,将导致化合物共价性的增加,极性减小,因而溶解度也降低。
水解
灼烧
金属硫化物在水中都会发生不同程度的水解:
S2-+ H2O ⇌ HS-+ OH-
HS-+ H2O ⇌ H2S + OH-
H2S的pKa分别约为:pKa1 = 6.89 和 pKa2 = 15±2, 因此金属硫化物溶液会呈不同程度的碱性,而碱金属的硫化物溶液的碱性更是可以与相应的氢氧化物匹敌。
氧化
灼烧硫化物矿物时可能发生两种反应:
硫化物转化为相应的氧化物,硫则转化为二氧化硫。例如由方铅矿制取铅时有一步为: 2PbS + 3O2→ 2PbO + 2SO2硫化物被氧化为相应的可溶硫酸盐。
以上两步都是冶炼金属时,转化硫化物矿石的重要方法。
硫化物酸碱性
硫化物中-2价的硫具有还原性,视条件不同可被氧化为硫、亚硫酸盐和硫酸盐等。
S2-- 2e-= S; -0.407V
重要的硫化物
硫化物和相应的氧化物类似,其酸碱性随周期和族的变化也和氧化物的类似,但硫化物的碱性不如氧化物强。
| H2S | NaHS | Na2S | As2S3 | As2S5 | Na2S2 |
| H2O | NaOH | Na2O | As2O3 | As2O5 | Na2O2 |
| \ | 碱性 | 碱性 | 两性 | 酸性 | 碱性 |
同周期元素最高氧化态硫化物从左到右酸性增强;同族元素相同氧化态的硫化物从上到下酸性减弱;同种元素的硫化物中,高氧化态的硫化物酸性更强。因此As2S5酸性强于Sb2S5,而Sb2S5的酸性则要强于SnS2和Sb2S3。[1]
多硫化物
| H2S | NaHS | Na2S | As2S3 | As2S5 | Na2S2 |
| H2O | NaOH | Na2O | As2O3 | As2O5 | Na2O2 |
| \ | 碱性 | 碱性 | 两性 | 酸性 | 碱性 |
硫化物的鉴定
硫化氢是一种无色有毒的气体,臭鸡蛋气味,空气中硫化氢的容许含量不超过0.01mg/L。硫化氢能够与人体的血红素中的亚铁离子结合生成硫化亚铁,使其失去反应活性。经常与硫化氢接触会引起嗅觉迟钝,消瘦,头痛等慢性中毒。实验室里常用金属硫化物与酸作用制备硫化氢。硫化氢的水溶液是氢硫酸,二元弱酸。无论在酸性介质还是碱性介质中,硫化氢的还原性都很强。[1]
硫化物来源
多硫化物是含有多硫离子Sn的化合物,n=2,3,4,5,6,...,9。多硫化物可由硫在硫化物溶液中煮沸制得,其溶液一般都为黄色,且颜色随n值的增加而加深。
多硫离子存在过硫键,类似于过氧化物,具有氧化性,但不及过氧离子氧化性强,反应发生歧化:
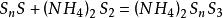
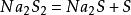
多硫化物在酸性溶液里很不稳定,酸化时即放出硫化氢和硫:
![]() + 2H → H2S + (n-1)S
+ 2H → H2S + (n-1)S
多硫离子还可作配体。例如Na2Sn作用于(η-C5H5)2TiCl2时,会生成含有TiS5环的配位化合物。[1]
硫化物的应用
点滴法点滴法是鉴定硫离子和硫氢根离子的灵敏方法,其步骤为:在点滴板上混合可溶硫化物的碱性溶液和1%的硝普酸钠Na2[Fe(CN)5NO](亚硝基铁氰化钠)溶液,若试样中存在S离子则会出现不同深度的红紫色,灵敏度1:50000。其机理是[Fe(CN)5(NOS)]4-离子的生成。 除此之外,向点滴板中加入试液、浓盐酸、几颗对氨基二甲基苯胺晶体和0.1mol/L氯化铁溶液,若在2~3分钟后出现蓝色,也可证明硫离子的存在。机理是生成了蓝色的亚甲基蓝。[1]
词条图册
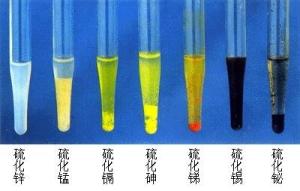 一些金属硫化物硫化物(sulfides)及其类似化合物包括一系列金属、半金属元素与S、Se、Te、As、Sb、Bi结合而成的矿物。矿物种数有350种左右,硫化物就占了2/3以上,其他为硒化物(selenides)、碲化物(tellurides)、砷化物(arsenides),及个别锑化物(antimonides)和铋化物(bismuthides)。
一些金属硫化物硫化物(sulfides)及其类似化合物包括一系列金属、半金属元素与S、Se、Te、As、Sb、Bi结合而成的矿物。矿物种数有350种左右,硫化物就占了2/3以上,其他为硒化物(selenides)、碲化物(tellurides)、砷化物(arsenides),及个别锑化物(antimonides)和铋化物(bismuthides)。
本大类矿物只占地壳总质量的0.15﹪,其中绝大部分为铁的硫化物,其他元素的硫化物及其类似类似化合物只相当于地壳总质量的0.001﹪。尽管其分布量有限,但却可以富集成具有工业意义的矿床,主要有有色金属,如Cu、Pb、Zn、Hg、Sb、Bi、Mo、Ni、Co等均以本大类矿物为主要来源,故本大类矿物在国民经济中具有重大意义。
依据成分中硫离子价态的不同和络阴离子的存在与否,硫化物矿物相应分为三类: 单硫化物:硫以S2-形式与阳离子结合而成,绝大多数为黑色; 过硫化物,硫以哑铃状对阴离子[S2]2-形式与阳离子结合而成;
硫盐矿物,硫与半金属元素砷、锑或铋组成锥状络阴离子[AsS3][2]

-
金属氧化物半导体场效应管
2025-09-20 18:27:43 查看详情


 求购
求购






