- 更昔洛韦

更昔洛韦
基本简介
基本信息
中文名称:更昔洛韦
中文别名:9-(1,3-二羟基-2-丙氧甲基)鸟嘌呤; 更昔洛韦水合物; 更息洛韦; 丙氧鸟苷
英文名称:ganciclovir
英文别名:biolf62; Ganciclovir; bw-759u; GVC; bwb759u;
CAS号:82410-32-0
分子式:C9H13N5O4
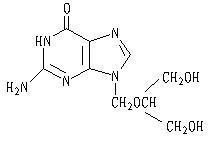 更昔洛韦结构式:
更昔洛韦结构式:
分子量:255.23100
精确质量:255.09700
PSA:139.28000
物化性质
外观与性状:白色粉末
密度:1.81 g/cm3
熔点:250°C
沸点:675ºC at 760 mmHg
稳定性:暴应避免露超过40ºC温度中。无菌粉末有3年的有效期限。
储存条件:2-8ºC
安全信息
符号:GHS08
信号词:危险
危害声明:H360
警示性声明:P201; P308 + P313
海关编码:2933990090
WGK Germany:3
危险类别码:R46; R60; R61
安全说明:S53-S36/37/39-S45
RTECS号:MF8407000
危险品标志:T[1]
生产方法
将化合物(I)(15 g,0.088 mo1)悬浮于200ml HMDS(1, 1, 1, 3, 3, 3-hexam.Ethyldisilizane)中,加入1.5 g硫酸铵,回流2h。反应液减压浓缩,往剩余的黄色固体加入氰化汞(24 g,0.095 mo1)和250 ml苯,加热至回流。加入6-氯鸟嘌呤(29.93 g,0.093 mo1)[1]
用途
适用于危及生命或视觉的巨细胞病毒(CMV)感染的免疫受损病人,如艾滋病、与器官移植和肿瘤化疗有关的外源性免疫抑制病人。用作抗病毒药物的中间体,用于治疗因免疫能力低下引起的巨细胞病毒(CMV)感染[1]。
实验分析
方法名称: 更昔洛韦原料药—更昔洛韦的测定—非水滴定法
应用范围: 本方法采用滴定法测定更昔洛韦原料药中更昔洛韦的含量。
本方法适用于更昔洛韦原料药。
方法原理: 供试品加冰醋酸溶解后,加结晶紫指示液,用高氯酸滴定液滴定至溶液显绿色,并将滴定的结果用空白试验校正,根据滴定液使用量,计算更昔洛韦的含量。
试剂: 1.冰醋酸
2.高氯酸滴定液(0.1mol/L)
3. 结晶紫指示液
4.基准邻苯二甲酸氢钾
仪器设备:
试样制备: 1. 高氯酸滴定液(0.1mol/L)
配制:取无水冰醋酸(按含水量计算,每1g水加醋酐5.22mL)750mL,加入高氯酸(70~72%)8.5mL,摇匀,放冷,加无水冰醋酸适量使成1000mL,摇匀,放置24小时。若所测供试品易乙酰化,则须用水分测定法测定本液的含水量,再用水和醋酐调节至本液的含水量为0.01%~0.2%。
标定:取在105℃干燥至恒重的基准邻苯二甲酸氢钾约0.16g,精密称定,加无水冰醋酸20mL使溶解,加结晶紫指示液1滴,用本液缓缓滴定至蓝色,并将滴定结果用空白试验校正。每1mL高氯酸滴定液(0.1mol/L)相当于20.42mg的邻苯二甲酸氢钾。根据本液的消耗量与邻苯二甲酸氢钾的取用量,算出本液的浓度。
2. 结晶紫指示液
取结晶紫0.5g,加冰醋酸100mL使溶解。
操作步骤: 精密称取供试品约0.15g,加冰醋酸40mL,加热使溶解,放冷,加结晶紫指示液1滴,用高氯酸滴定液(0.1mol/L)滴定至溶液显绿色,并将滴定的结果用空白试验校正。每1mL高氯酸滴定液(0.1mol/L)相当于25.52mg的C9H13N5O4。
注:“精密称取”系指称取重量应准确至所称取重量的千分之一。“精密量取”系指量取体积的准确度应符合国家标准中对该体积移液管的精度要求。
药典标准
来源含量
本品为9-[[2-羟基-1-(羟甲基)乙氧基]甲基]鸟嘌呤。按干燥品计算,含C9H13N5O4不得少于99.0%。
性状
本品为白色结晶性粉末;无臭,无味;有引湿性。
本品在水或冰醋酸中微溶,在甲醇中几乎不溶,在二氯甲烷中不溶;在盐酸溶液或氢氧化钠溶液中略溶。
鉴别
(1)取本品适量,加水溶解并稀释制成每1ml中约含10μg的溶液,照紫外-可见分光光度法(2010年版药典二部附录ⅣA)测定,在252nm的波长处有最大吸收;在222nm的波长处有最小吸收。
(2)本品的红外光吸收图谱应与对照品的图谱一致(2010年版药典二部附录Ⅳ C)。如不一致,取本品和对照品适量,分别加水制成饱和溶液,滤过,取滤液在10℃以下放置过夜,待析出结晶,滤过,滤渣经105℃干燥后,再次测定。
检查
有关物质
取本品15mg,精密称定,置50ml量瓶中,加0.4%氢氧化钠溶液1ml使溶解,用流动相稀释至刻度,摇匀,作为供试品溶液;精密量取1ml,置100ml量瓶中,用流动相稀释至刻度,摇匀,作为对照溶液。照高效液相色谱法(2010年版药典二部附录ⅤD)测定,用十八烷基硅烷键合硅胶为填充剂,以甲醇-水(5:95)为流动相,检测波长为252nm;理论板数按更昔洛韦峰计算不低于3000。取对照溶液20μl,注入液相色谱仪,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的15%。精密量取供试品溶液和对照溶液各20μl,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的2倍。供试品溶液的色谱图中如有杂质峰,各杂质峰面积的和不得大于对照溶液的主峰面积(1.0%)。
干燥失重
取本品,在105℃干燥至恒重,减失重量不得过6.0%(2010年版药典二部附录ⅧL)。
炽灼残渣
取本品1.0g,依法检查(2010年版药典二部附录Ⅷ N),遗留残渣不得过0.1%。
重金属
取炽灼残渣项下遗留的残渣,依法检查(2010年版药典二部附录ⅦH第二法),含重金属不得过百万分之十。
含量测定
取本品约0.15g,精密称定,加冰醋酸40ml,加热使溶解,放冷,加结晶紫指示液1滴,用高氯酸滴定液(0.1mol/L)滴定至溶液显绿色,并将滴定的结果用空白试验校正。每1ml的高氯酸滴定液(0.1mol/L)相当于25.52mg的C9H13N5O4。
类别
抗病毒药。
贮藏
遮光,密封保存。
制剂
(1)更昔洛韦氯化钠注射液(2)注射用更昔洛韦
药物说明
药理毒理
细胞内的丙氧鸟苷经脱氧鸟苷激酶作用被磷酸化为丙氧鸟苷的一价磷酸盐,也可被一些细胞激酶进一步磷酸化为三价磷酸盐,在被巨细胞病毒感染的细胞内丙氧鸟苷可被优先磷酸化。丙氧鸟苷三价磷酸盐的代谢非常缓慢,从细胞外液分离后18 hr尚可保存 60~70%。其抑制病毒DNA合成的机制在于1.竞争抑制脱氧鸟苷的三价磷酸盐与DNA聚合酶的结合,2.丙氧鸟苷的三价磷酸盐与病毒DNA的结合最终导致DNA延长的停止。从接受本药治疗的巨细胞病毒感染患者中发现,巨细胞病毒可以产生急性抗药性。丙氧鸟苷是化学合成的鸟嘌呤类似物,能够阻止疱疹病毒的复制。对其敏感的病毒包括CMV,HSV-1,HSV-2,EBV,VZV。临床研究仅限于对巨细胞病毒感染患者疗效的评价。
药动学
本药主要是通过肾小球滤过作用以原型排出。肾功能正常的患者,以5 mg/kg体重的剂量持续注射1 hr后,其半衰期为2.9 hr,平均清除率为3.64 mL/分/kg体重。以5 mg/kg体重的剂量,每日注射2次,14天后未引起药物积蓄。肾功能不全的患者,血肌酐含量分别为<124 mmoL/L、125~225 mmol/L及226~398 mmoL/L时,药物血浆清除率和半衰期分别为3.64 mL/分/kg体重和2.9 hr,2.01 mL/分/kg体重和5.3 hr及1.11 mL/分/kg体重和9.7 hr。严重肾功能受损的患者,血液透析可使药物浓度降低50%。
适应症
严重免疫功能低下所致的盲性巨细胞病毒性视网膜炎、艾滋病、器管移植、恶性肿瘤等,以及肺炎、胃肠炎、肝脏和中枢神经系统CMV感染。
不良反应
白细胞及血小板减少最常见,少见的有贫血,发热,皮疹,肝功能异常,浮肿,感染,乏力。心律失常,高/低血压。思维异常或恶梦,共济失调,昏迷,头昏,头痛,紧张,感觉障碍,精神病,嗜睡,震颤。恶心,呕吐,腹泻,胃肠道出血,腹痛。嗜曙红细胞增多,低血糖。呼吸困难。脱发,瘙痒,荨麻疹。血尿及尿素氮升高。有巨细胞病毒感染性视网膜炎的艾滋病患者可出现视网膜剥离。注射处可见感染,疼痛,静脉炎。
药物相互作用
丙磺舒以及其它一些可以抑制肾小管分泌和重吸收的药物,能降低肾脏对本药的清除率及延长其半衰期。本药与抑制细胞快速分裂复制的药物同时使用可产生协同效应。本药与氨苯砜,戊烷脒,氟胞咪啶,长春新碱,长春花碱,阿霉素,两性霉素,三甲氧基氨嘧啶以及一些核苷类药物联合使用,可增加副作用的发生。艾滋病患者同时使用本药和齐多夫定,大多会产生严重的白细胞降低。本药与伊米配能/西司他丁钠盐联合使用可诱发癫痫。
用法用量
 更昔洛韦巨细胞病毒感染的治疗 预防和诱导期:5 mg/kg体重/次,每日2次静脉注射,每次注射时间应超过1 hr,维持14~21天。维持期:6 mg/kg体重/日,每周5天或5 mg/kg体重/日,每周7天,静脉注射。当患者的视网膜炎有进一步发展时,需要再次使用诱导剂量进行治疗。
更昔洛韦巨细胞病毒感染的治疗 预防和诱导期:5 mg/kg体重/次,每日2次静脉注射,每次注射时间应超过1 hr,维持14~21天。维持期:6 mg/kg体重/日,每周5天或5 mg/kg体重/日,每周7天,静脉注射。当患者的视网膜炎有进一步发展时,需要再次使用诱导剂量进行治疗。
巨细胞病毒感染性疾病的预防 诱导量5 mg/kg体重,每12 hr注射1次,维持7~14天。
当患者肾功能不全时,诱导剂量应调整如下:血肌酐<124 μmoL/L者,剂量不变;血肌酐为125~225μmoL/L时,使用2.5 mg/Kg体重,每日2次的剂量 ;血肌酐为226~398 μmoL/L时,剂量为2.5 mg/kg体重,每日1次 ;血肌酐>398 μmoL/L时,剂量为1.25 mg/kg体重,每日1次。其最佳维持剂量尚不明确,透析患者的用药剂量为1.25 mg/kg体重/日。一天的透析结束后应立即用药。 症状 500 mg/kg对动物一次性静脉注射可产生呕吐、唾液分泌过多、出血、迟纯、肝功能异常、尿素氮升高、睾丸萎缩、死亡。治疗 血液透析及增加补液可降低药物血浆浓度。 每小瓶应加入10 mL注射用水,其配制溶液浓度为50 mg/mL,将药物加入100 mL静脉注射液中,注射时间应超过1 hr。0.9%生理盐水,5%葡萄糖,乳酸钠注射液及林格氏液可以与本药配伍,含有对羟基甲酸盐成分的抗菌素溶液与本药不相容。稀释后的注射用液应当冷藏但不能冷冻,而且必需在24 hr内使用[2]。
注意事项
怀孕及哺乳期妇女,对本药或阿昔洛韦过敏者禁用。 致癌、致畸性及对生育能力影响 临床前期研究发现,本药可以引起精子减少,突变,致畸及致癌,在停止治疗的90天内应采取避孕措施。大约10~40%接受治疗的患者出现白细胞减少,因此本药应慎用于有白细胞减少病史的患者。10%接受本药治疗的患者出现血小板减少(少于5万个/L),接受免疫抑制药物治疗的患者比艾滋病患者下降得更低。当患者的血小板计数少于10万个/L时,发生血小板减少的风险也增大。
对妊娠和哺乳的影响 动物实验发现本药有致畸作用,怀孕期妇女不能使用。本药对哺乳动物的后代可产生不良影响。目前尚不知本药是否能分泌到人乳中,故不能在哺乳妇女中使用,使用本药72 hr后才能恢复哺乳。
对儿童的影响 应用于12岁以下儿童的临床经验有限,故儿童应慎用。据报道其不良后果与成人相似。
对老年人的影响 应按肾功能情况调整用药剂量[2]。
生产
生产单位是上海罗氏制药有限公司
关于更昔洛韦的合成,文献中报道的方法很多,但基本合成原理是一致的,1982年至今,先后有多家公司申请更昔洛韦合成工艺专利,但基本上都是以嘌呤及其衍生物为主要原料与各种被保护的2-羟甲基甘油进行缩合反应,然后脱除保护制得。也有通过环合反应制得更昔洛韦的报道,但通过环合路线合成更昔洛韦原料难得,工艺条件复杂,收率低从而失去工业化意义。
根据主要原料不同,合成更昔洛韦的方法主要有5种,分别是加拿大ENS Biol公司、美国Syntex公司、美国Merck公司、英国Wellcome基金有限公司、西班牙Inke公司所持有[2]。

-
索洛韦茨基群岛的文化历史建筑群
2025-09-22 12:01:35 查看详情


 求购
求购






