- 蛋氨酸

蛋氨酸
理化性质
外观与性状:白色薄片状结晶或结晶性粉末。有特殊气味。味微甜。
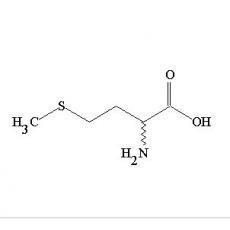 甲硫氨酸(2)熔点:280~281℃(分解)(L体);281℃(消旋体)
甲硫氨酸(2)熔点:280~281℃(分解)(L体);281℃(消旋体)
酸碱性:10%水溶液的PH值5.6~6.1。
旋光性:无旋光性。
稳定性:对热及空气稳定。对强酸不稳定,可导致脱甲基作用。
溶解性:溶于水(3.3g/100ml,25℃)、稀酸和稀碱。极微溶于95%的乙醇,极难溶于无水乙醇,几乎不溶于乙醚。
相对密度(水=1):1.340(消旋体)
制备
⒈可用酪蛋白经水解、精制而得。
⒉也可由甲硫醇与丙烯醛经斯特雷克合成反应制备(由甲硫醇和丙烯醛加成后再与氰化钠和氯化铵反应,生成a-氨基腈,再经水解得到a-氨基酸)。
作用用途
DL-蛋氨酸(DL-Methionine)用途:
营养增补剂。与L-型蛋氨酸的生理效果相同,但价格低(L-型由DL-型制得),故一般均用DL-蛋氨酸。在燕麦、黑麦、米、玉米、小麦、花生粉、大豆、土豆、菠菜等植物性食品中属于限制氨基酸。添于上述食品中以改善氨基酸平衡。需要量随胱氨酸摄入量而异。成人男子需要量为1.1g/d。
海胆味与蛋氨酸有关,海胆甜味与甘氨酸、丙氨酸有关,苦味与缬氨酸有关,鲜味与谷氨酸等有关,因此可将这些氨基酸配制成调味剂。
尚用于氨基酸输液,综合氨基酸制剂。
按我国GB2760-86规定可用作香料。
肝脏保护
抗肝硬变、脂肪肝及各种急性、慢性、病毒性、黄疸性肝。
甲硫氨酸可以促进肝细胞膜磷脂甲基化,使膜流动性增强Na+、K+-ATP酶泵作用强,可以减少肝细胞内胆汁的淤积,转硫基作用加强,从而增强了肝细胞内半胱氨酸、谷胱苷肽及牛磺酸的合成,减少了胆汁酸在肝内聚积,加强了解毒作用,有利于肝细胞恢复正常生理功能,促使黄疸消退和肝功能恢复。
抗各种原因引起的肝内胆汁淤积病毒感染、妊娠和长期肠道外营养都有可能导致肝内胆汁淤积,甲硫氨酸通过生成牛磺酸与胆汁酸共价结合,增强酸溶解度,易于排除肝细胞外,同时通过肝细胞膜磷的甲基化,增强Na+、K+、-ATP酶活性促进胆汁外排。
应用甲硫氨酸可以明显减少由胆汁淤积引起的皮肤瘙痒和肝功异常。
心肌保护
甲硫氨酸通过增加体内半胱氨酸和谷胱苷肽合成,增加谷胱苷肽过氧化物酶和超氧歧化酶活性,其甲基作用使内源性磷脂合成增加,从而稳定了溶酶体膜,减少了酸性磷酸酶的释放,保护了心肌细胞线粒体免受损害,对克山病造成的心肌损害尤为有用。
抗抑郁症
抑郁症患者血液中甲硫氨酸浓度显著降低补充外源性甲硫氨酸对抑郁症有治疗作用。
降血压
甲硫氨酸通过转硫作用生成牛磺酸有明显的降压作用。
防毒袪毒
甲硫氨酸能预防和治疗有毒金属非金属对人体的伤害。
甲硫氨酸利用其所带的甲基,在体内转化成谷胱苷肽,对有毒物或药物进行甲基化而起到解毒的作用。因此,甲硫氨酸可用于防治慢性或急性肝炎、肝硬化等肝脏疾病,也可用于缓解砷、三氯甲烷、四氯化碳、苯、吡啶和喹啉等有害物质的毒性反应。是预防和治疗重金属铅镉汞对机体造成损害的重要物质。
它与进入人体内的毒性金属结合,变成可溶性的物质随胆汁排除体外,发挥了防毒和驱毒作用。人体肺部沾染SiO2粉尘后,组织释放氧自由基增加造成脂质过氧化增加,造成肺脏进一步损害,甲硫氨酸转化成的半胱氨酸和谷胱苷肽可以阴断这一过程,保护肺部免受进一步损害。
人体代谢
甲基化在体内生物合成与代谢中发挥着重要的作用。甲硫氨酸是体内最重要的甲基供体,很多含氮物质在生物合成时甲硫氨酸提供甲基如肌酸、松果素、肾上腺素、肉碱、肌碱、胆碱、甲基组胺、甲菸胺等。同样甲基化在蛋白质和核酸的修饰加工方面也极为重要。
其他
含蛋氨酸的食物不像其他营养素那么的多,其中含量最丰富的前几位食物有:芝麻、葵花子、乳制品、酵母、海藻类、叶类蔬菜等。
该品与甘氨酸有拮抗作用,禽兽缺乏甲硫氨酸会引起发育不良、体重减轻、肝肾机能减弱、肌肉萎缩、皮毛变质等。
甲硫氨酸脑啡肽具有多种生理活性。甲硫脑啡肽能够增强TNFa产生和NK细胞活性。增强介素IL-1、IL-2、IL-6的表达。能够减轻肝细胞损伤对淋巴细胞增强的抑制,参与了调整月经周期,同时甲硫脑啡肽与5-羟色胺以串联方式发挥中枢镇痛作用。
规格指标
L-甲硫氨酸 中国药典2010版
| Test Items项目 | Specification质量指标 |
| Assay 含量 | ≥98.5% |
| Characteristic性状 | 白色结晶或结晶性粉末,有特臭。 |
| Specific rotation[a]D比旋度 | +21.0°~ +25.0° |
| Identification 鉴别 | 该品的红外吸收图谱与对照图谱(光谱集444图)一致 |
| PH酸度 | 5.6~6.1 |
| Transmittance溶液透光率 | ≥98.0% |
| Chloride氯化物 | ≤0.02% |
| Sulfate硫酸盐 | ≤0.02% |
| Ammonium铵盐 | ≤0.02% |
| Other amino acids其他氨基酸 | ≤0.5% |
| Loss on drying干燥失重 | ≤0.2% |
| Residue on ignition炽灼残渣 | ≤0.1% |
| Iron铁盐 | ≤0.0015% |
| Heavy metals(as Pb)重金属 | ≤10ppm |
| Arsenic砷盐 | ≤0.0001% |
| Bacterial endotoxins细菌内毒素 | ≤25 EU/g |
Storage:Preserve in well-closed containers密封保存
化学分析
| Test Items项目 | Specification质量指标 |
| Assay 含量 | ≥98.5% |
| Characteristic性状 | 白色结晶或结晶性粉末,有特臭。 |
| Specific rotation[a]D比旋度 | +21.0°~ +25.0° |
| Identification 鉴别 | 该品的红外吸收图谱与对照图谱(光谱集444图)一致 |
| PH酸度 | 5.6~6.1 |
| Transmittance溶液透光率 | ≥98.0% |
| Chloride氯化物 | ≤0.02% |
| Sulfate硫酸盐 | ≤0.02% |
| Ammonium铵盐 | ≤0.02% |
| Other amino acids其他氨基酸 | ≤0.5% |
| Loss on drying干燥失重 | ≤0.2% |
| Residue on ignition炽灼残渣 | ≤0.1% |
| Iron铁盐 | ≤0.0015% |
| Heavy metals(as Pb)重金属 | ≤10ppm |
| Arsenic砷盐 | ≤0.0001% |
| Bacterial endotoxins细菌内毒素 | ≤25 EU/g |
性状检验
含量测定
酸度测定:取该品0.5g,加水50ml溶解后,依法测定,pH值应为5.6~6.1。
溶液的透光度:取该品0.5g,加水20ml溶解后,照分光光度法,在430nm的波长处测定透光率,不得低于98.0%。
氯化物检验:取该品0.30g,依法检查,与标准氯化钠溶液6.0ml制成的对照液比较,不得更浓(0.02%)。
硫酸盐检验:取该品1.0g,依法检查,与标准硫酸钾溶液2.0ml制成的对照液比较,不得(0.02%)。
铵盐检验:取该品0.10g,依法检查,与标准氯化铵溶液2.0ml制成的对照液比较,不得更深(0.02%)。
其他氨基酸测定:取该品,加水制成每1ml中含10mg的溶液,照薄层色谱法试验,吸取上述溶液5μl,点于硅胶G薄层板上,以正丁醇-冰醋酸-水(4:1:5)为展开剂,展开后,晾干,在90℃干燥10分钟,喷以茚三酮的丙酮溶液(0.5→100),再在90℃加热10分钟,立即检视,应只显一个紫色斑点。
干燥失重:取该品,在105℃干燥3小时,减失重量不得过0.2%。炽灼残渣 不得过0.1%。铁盐 取该品1.0g,依法检查,与标准铁溶液1.5ml制成的对照液比较,不得更深(0.0015%)。重金属 取该品0.50g,加水23ml溶解后,加醋酸盐缓冲液(PH3.5)2ml,依法检查,含重金属不得过百万分之十。砷盐 取该品2.0g,加水23ml溶解后,加盐酸5ml,依法检查,应符合规定(0.0001%)。
热原测定:取该品,加氯化钠注射液制成每1ml中含20mg的溶液,依法检查,剂量按家兔体重每1kg注射10ml,应符合规定(供注射用)。
代谢分析
方法名称:甲硫氨酸原料药—甲硫氨酸的测定—电位滴定法
应用范围:该方法采用滴定法测定甲硫氨酸原料药中甲硫氨酸的含量。该方法适用于甲硫氨酸原料药。
方法原理:供试品加无水甲酸与冰醋酸溶解后,,用高氯酸滴定液进行电位滴定,并将滴定的结果用空白试验校正,根据滴定液使用量,计算甲硫氨酸的含量。
试剂:
⒈冰醋酸
⒉ 无水甲酸
⒊ 高氯酸滴定液(0.1mol/L)
⒋ 结晶紫指示液
⒌ 基准邻苯二甲酸氢钾
仪器设备:电位滴定仪
试样制备:
①高氯酸滴定液(0.1mol/L)
配制:取无水冰醋酸(按含水量计算,每1g水加醋酐5.22mL)750mL,加入高氯酸(70~72%)8.5mL,摇匀,放冷,加无水冰醋酸适量使成1000mL,摇匀,放置24小时。若所测供试品易乙酰化,则须用水分测定法测定本液的含水量,再用水和醋酐调节至本液的含水量为0.01%~0.2%。
标定:取在105℃干燥至恒重的基准邻苯二甲酸氢钾约0.16g,精密称定,加无水冰醋酸20mL使溶解,加结晶紫指示液1滴,用本液缓缓滴定至蓝色,并将滴定结果用空白试验校正。每1mL高氯酸滴定液(0.1mol/L)相当于20.42mg的邻苯二甲酸氢钾。根据本液的消耗量与邻苯二甲酸氢钾的取用量,算出本液的浓度。
②结晶紫指示液
取结晶紫0.5g,加冰醋酸100mL使溶解。
操作步骤:精密称取供试品约0.13g,加无水甲酸3mL与冰醋酸50mL溶解后,照电位滴定法,用高氯酸滴定液(0.1mol/L)滴定,并将滴定的结果用空白试验校正。每1mL高氯酸滴定液(0.1mol/L)相当于14.92mg的C5H11NO2S。
注:“精密称取”系指称取重量应准确至所称取重量的千分之一。“精密量取”系指量取体积的准确度应符合国家标准中对该体积移液管的精度要求。
词条图册
甲硫氨酸,为含硫α-氨基酸之一。是蛋白质的一种成分,卵白蛋白和酪蛋白中很多,天然得到的是L-型。是必需氨基酸之一,L型D型都有效。或直接脱去甲硫醇和氨,而间接地经同型半胱氨酸分解成α-酮酸。甲硫氨酸的生物合成是从O-乙酰同型丝氨酸等硫化物,或由半胱氨酸的逆途径生成同型半胱氨酸(至此仅在链孢霉上出现),再向同型半胱氨酸通过转移甲基而生成。
这些甲基有由⑴N-最高正价化合物(例如甜菜碱),⑵ S-最高正价化合物(例如硫代甜菜碱)直接转移的,有由⑶活性C1单位新产生的等。再者活性甲硫氨酸本身,也通过分解成同型半胱氨酸,成为肌酸、N-甲基烟酸、胆碱、甲基组氨酸等的甲基供体。
活性甲硫氨酸经过脱羧、脱硫甲基反应也变成多胺。另一条合成途径是通过硫甲基转移给α-酮丁酸而生成甲硫氨酸。甲硫氨酸含的硫对碱是稳定的。溴化氰在甲硫氨酸残基处可将肽切断,因此多用于氨基酸排列的研究。甲硫氨酸为人体必需八种氨基酸之一。人体内不能合成,必须依靠外源补充。甲硫氨酸在人体内与ATP结合生成S-腺苷氨酸。

-
2-氨基-5-氯嘧啶
2025-09-29 02:20:53 查看详情


 求购
求购









