- 苯并芘

苯并芘
基本介绍
 苯并芘(3)苯并芘(Benzopyrene)是苯与芘稠合而成的一类多环芳烃。根据稠合的位置不同,可以有苯并[a]芘和苯并[e]芘两种异构体,这两个名称来源于IUPAC命名法中对芘分子环中各化学键的编号。
苯并芘(3)苯并芘(Benzopyrene)是苯与芘稠合而成的一类多环芳烃。根据稠合的位置不同,可以有苯并[a]芘和苯并[e]芘两种异构体,这两个名称来源于IUPAC命名法中对芘分子环中各化学键的编号。
最常见的苯并芘是苯并[a]芘。它是一种致癌物质和突变原。
苯并芘(běn bìng bǐ)是一类具有明显致癌作用的有机化合物。它是由一个苯环和一个芘分子结合而成的多环芳烃类化合物。
目前已经检查出的400多种主要致癌物中,一半以上是属于多环芳烃一类的化合物。其中,苯并芘则是一种强致癌物。
吸烟烟雾和经过多次使用的高温植物油、煮焦的食物、油炸过火的食品都会产生苯并芘。
对于苯并芘,日本人曾将其在兔子身上做过实验。实验表明,将苯并芘涂在兔子的耳朵上,涂到第40天,兔子耳朵上便长出了肿瘤。
研究证明,生活环境中的苯并芘含量每增加1%时,肺癌的死亡率即上升5%。[2]
理化常数
化合物类别:芳烃类
分子式:C 20H 12
外观与性状:无色至淡黄色、针状、 晶体(纯品)
分子量:252.32
蒸汽压:0.665×10-19kPa/25℃
熔点:179℃ 沸点:475℃ 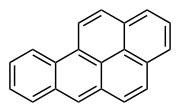 苯并芘
苯并芘
溶解性:不溶于水,微溶于 乙醇、 甲醇,溶于苯、甲苯、二甲苯、 氯仿、 乙醚、丙酮等
密度:相对密度(水=1)1.35
稳定性:稳定
主要用途:本品在工业上无生产和使用价值,一般只作为生产过程中形成的副产物随废气排放。
化学性质
存在于主流烟气中、侧流烟气中。有毒。 IARC致癌性评估:证据充分,引发活性。
组织化学测定脂类(呈蓝或蓝白色荧光,褪色快,不能作永久标本)。癌症的研究。
代谢和降解
据有关资料显示,BaP在哺乳动物体内的代谢和降解产物主要是:1,2-二羟基-1,2-二氢苯并芘,9,10-二羟基-9,10-二氢苯并芘,6羟基苯并,3羟基苯并芘,1,6-二羟基苯并芘,3,6-二羟基苯芘,苯并芘二酮,苯并芘-3,6-二酮(IRPTC)。另外还有苯并芘-1,6-二酮,11羟基苯并芘,苯并芘-7,8-二氢二醇(Lehr.R.E.1978)。
BaP在大气中的化学半衰期在有日光照射下少于1天,没有日光照射时要数天,水体表层中的BaP在强烈照射下半衰期为几小时至十几小时。众多研究实验表明,中高浓度苯并芘(10-200mg/kg之间)的生物降解为零级反应,42天降解约80%的苯并芘 [3] 。对于低浓度苯并芘(10mg/kg以下)的生物降解为一级反应,类似自然条件下(含水率22%)半衰期为93天,在类似泥浆反应器中(含水率65%)半衰期为33天 。
残留与蓄积
在水体,土壤和作物中BaP都容易残留。许多国家都进行过土壤中BaP含量调查,残留浓度取决于污染原的性质与距离,在繁忙的公路两旁的土壤中BaP含量为2.0mg/kg,在炼油厂附近土壤中是200mg/kg;被煤 焦油, 沥青污染的土壤中,可以高达650mg/kg,食物中的BaP残留浓度取决于附近是否有工业区或交通要道。进入食物链的量决定于烹调方法,不适当的油炸可能使BaP含量升高,但进入人体组织后,分解速度比较快。水中的BaP主要是由于工业“ 三废”排放。残留时间一般不太长,特别在阳光和微生物影响下,数小时内就被 代谢和降解。水生生物对BaP的 富集系数不高,在0.1μg/L浓度水中鱼对BaP的 富集系数35天为61倍,清除75%的时间为5天。
迁移转化
BaP存在于煤焦油、各类炭黑和煤、及焦化、炼油,沥青、塑料等工业污水中。肉和鱼中的BaP含量取决于烹调方法,水果、蔬菜和粮食中的BaP含量取决其来源。主要来自洗刷大气的雨水水中的BaP以吸附于某些 颗粒上、溶解于水中和呈胶体状态等三种形式存在,其中大部分吸附在 颗粒物质上。日光照射下,大气中的BaP化学 半衰期不足24小时,没有日光照射为数日。水中的BaP在强烈日光照射下半衰期为几小时至十几小时,土壤中BaP的降解速度8天约为53%~82%;对 酸碱较稳定,日光照射能促使分解,速度加快。水体,进入人体后,分解速度比较快。水中的BaP主要来自工业排放。BaP被认为是高活性致癌剂,但并非 直接致癌物,必须经细胞微粒体中的混合功能氧化酶激活才具有致癌性。BaP不仅广泛存在于环境中,而且与其它多环芳烃的含量不一定的相关性,长期生活在含BaP的空气环境中会造成慢性中毒。许多国家的动物实验证明,BaP具有致癌、致畸、致突变性。 危险特性,遇明火、高热可燃。受高热分解放出有毒的 气体。
燃烧(分解)产物:完全燃烧得到水和 二氧化碳、成分未知的黑色烟雾。不完全燃烧就有有毒的 一氧化碳!
相关影响
健康危害
侵入途径:吸入、食入、经皮吸收。
健康危害:对 眼睛、 皮肤有刺激作用。是致 癌物、致畸原及 诱变剂。
毒理学资料及环境行为 毒性:是 多环芳烃中毒性最大的一种强烈致癌物。
急性毒性
LD50500mg/kg(小鼠腹腔);50mg/kg(大鼠皮下)
慢性毒性:长期生活在含BaP的空气环境中,会造,空气中的 BaP是导致肺癌的最重要的因素之一。
水生生物毒性:5μg/L,12天,微生物,阻碍作用;5mg/L,13小时,软体动物卵,阻碍作用,结构变化。
致癌
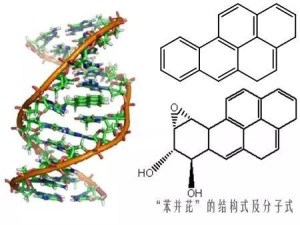
 苯并芘BaP被认为是高活性致癌剂,但并非直接致癌物,必须经细胞微粒体中的 混合功能氧化酶激活才具有致癌性。BaP进入机体后,除少部分以原形随粪便排出外,一部分经肝、肺细胞微粒体中混合功能 氧化酶激活而转化为数十种代谢产物,其中转化为 羟基化合物或醌类者,是一种解毒反应;转化为环 氧化物者,特别是转化成7,8-环氧化物,则是一种活化反应,7,8-环氧化物再代谢产生 7,8-二氢二羟基-9,10-环氧化苯并[a]芘 (如图),便可能是最终致癌物。这种最终致癌物有四种异构体,其中的(+)-BP-7β,8α-二醇体-9α,10α-环氧化物-苯并[a]芘,已证明致癌性最强,它与 DNA形成 共价键结合,造成DNA损伤,如果DNA不能修复或修而不复,细胞就可能发生癌变。其它三种异构体也有致癌作用。动物试验包括经口、经皮、吸入,经腹膜皮下注射、均出现致癌。许多国家相继用9种动物进行实验,采用多种给药途径,结果都得到诱发癌的阳性报告。在多环芳烃中,BaP污染最广、致癌性最强。BaP不仅在环境中广泛存在,也较稳定,而且与其它多环芳烃的含量有一定的相关性,所以,一般都把BaP作为大气致癌物的代表。
苯并芘BaP被认为是高活性致癌剂,但并非直接致癌物,必须经细胞微粒体中的 混合功能氧化酶激活才具有致癌性。BaP进入机体后,除少部分以原形随粪便排出外,一部分经肝、肺细胞微粒体中混合功能 氧化酶激活而转化为数十种代谢产物,其中转化为 羟基化合物或醌类者,是一种解毒反应;转化为环 氧化物者,特别是转化成7,8-环氧化物,则是一种活化反应,7,8-环氧化物再代谢产生 7,8-二氢二羟基-9,10-环氧化苯并[a]芘 (如图),便可能是最终致癌物。这种最终致癌物有四种异构体,其中的(+)-BP-7β,8α-二醇体-9α,10α-环氧化物-苯并[a]芘,已证明致癌性最强,它与 DNA形成 共价键结合,造成DNA损伤,如果DNA不能修复或修而不复,细胞就可能发生癌变。其它三种异构体也有致癌作用。动物试验包括经口、经皮、吸入,经腹膜皮下注射、均出现致癌。许多国家相继用9种动物进行实验,采用多种给药途径,结果都得到诱发癌的阳性报告。在多环芳烃中,BaP污染最广、致癌性最强。BaP不仅在环境中广泛存在,也较稳定,而且与其它多环芳烃的含量有一定的相关性,所以,一般都把BaP作为大气致癌物的代表。
致畸
1000mg/kg,妊娠大鼠以口,胎儿致畸。
致DNA突变
40mg/kg,1次,田鼠经腹膜,染色体试验多种变化。小鼠, 遗传表型试验 多种变化。昆虫,微生物,遗传表型试验多种变化。人体细胞培养DNA多种变化。
污染来源
存在于煤焦油、各类碳黑和煤、石油等燃烧产生的烟气、香烟烟雾、 汽车尾气中,以及焦化、炼油、 沥青、塑料等工业污水中。地面水中的BaP除了工业排污外,主要来自洗刷大气的雨水。储水槽及管道涂层淋溶。
食品中苯并芘化合物主要来源于:熏烤或高温烹调时使食品污染苯并芘;食品加工过程中受到有污染;沥青污染;包转材料污染;环境污染等 [4] 。
预防措施
减少环境污染,食品中苯并芘的污染源主要来自于环境;改进食品加工方法,熏制和烘烤食品时,改进燃烧过程,避免食品直接接触炭火,改进熏烟工艺等;去毒,对已经造成苯并芘污染的食品可采取不同的措施去毒,如活性炭吸附去毒;制定食品中苯并芘的限量标准 [4] 。
处置方法
 苯并芘一、 泄漏应急处理隔离泄漏污染区,周围设警告标志,应急处理人员戴自给式呼吸器,穿化学防护服。不要直接接触泄漏物,避免扬尘,小心扫起,用 水泥、沥青或适当的 热塑性材料固化处理再废弃。如大量泄漏,收集回收或无害处理后废弃。
苯并芘一、 泄漏应急处理隔离泄漏污染区,周围设警告标志,应急处理人员戴自给式呼吸器,穿化学防护服。不要直接接触泄漏物,避免扬尘,小心扫起,用 水泥、沥青或适当的 热塑性材料固化处理再废弃。如大量泄漏,收集回收或无害处理后废弃。
二、防护措施 呼吸系统防护:一般不需特殊防护,但建议特殊情况下,佩带 自给式呼吸器。
眼睛防护:戴 安全防护眼镜。
防护服:穿 聚乙烯薄膜防毒服。
手防护:必要时戴防 化学品手套。
其它:工作后,淋浴更衣。避免长期反复接触。谨防其致癌性。 三、急救措施 皮肤接触:脱去污染的衣着,用肥皂水及清水彻底冲洗。
眼睛接触:立即翻开上下眼睑,用流动清水冲洗15分钟。就医。
吸入:脱离污染环境,用水漱洗鼻咽部的 粉尘。就医。
食入:误服者充分漱口、饮水,催吐。就医。 灭火方法:二氧化碳、 干粉、 1211灭火剂、砂土。用水可引起沸溅。
研究进展
 苯并芘多环芳烃(PAHs)是一类由两个或两个以上芳香环构成的化合物,在自然环境中分布极其广泛。由于多数PAHs具有 致癌性、致畸性,受到广泛的关注。微生物修复技术是去除多环芳烃污染环境的最佳方法,它不仅经济、安全,而且所能处理的阈值低、残留少,其应用前景十分广阔。
苯并芘多环芳烃(PAHs)是一类由两个或两个以上芳香环构成的化合物,在自然环境中分布极其广泛。由于多数PAHs具有 致癌性、致畸性,受到广泛的关注。微生物修复技术是去除多环芳烃污染环境的最佳方法,它不仅经济、安全,而且所能处理的阈值低、残留少,其应用前景十分广阔。
研究设计并测定了几种菌株对高分子量多环芳烃苯并芘(Bap)的最佳降解条件。结果表明在浓度为80mg/L、pH值为7.2、代谢底物为邻苯二甲酸的最佳条件下,2<'#>真菌(木霉)、6<'#>真菌(镰刀霉)、9<'#>细菌(动胶杆菌)降解苯并芘的降解率分别达到81.7%、85.7%、87.8%,而且降解速度较快,菌株生物量较高,可以进一步应用于多环芳烃的细菌的 固定化处理系统以及土壤中多环芳烃的降解,并为研究苯并芘降解途径、 分离纯化 次生代谢产物建立了基础。
高分子量多环芳烃的降解通常以共代谢方式进行,比较了联苯、水杨酸、 邻苯二甲酸、琥珀酸钠四种常用底物对于苯并芘的共代谢降解效果。研究表明:以邻苯二甲酸作为 共代谢底物时,上述3种菌株的降解效果较好。此外,对非离子表面活性Tween-80增溶条件下,苯并芘的生物降解作了初步的研究。
检测方法
高效液相色谱-荧光法
高效液相色谱法简称HPLC,这种检测技术是20世纪60年代后期才发展出来的,该方法具有相对比较新颖、精确度较高、良好的重复性、分辨率相对较高的优点。荧光法具有能够提高检测的灵敏度、具有良好的选择性等优点,可以将同分异构体很好的分离开来,有利于检测目标物的准确定量。因此,两者结合在一起,能够进一步提高对苯并芘检测的精度和准确率。例如:李念念、周光宏等用HPLC对腊肉中的苯并芘进行测定,检出限和定量限可达0.15和0.5 ug/Kg。程威威、汪学德等也用此方法对芝麻油中的Bap进行检测;与国标相比,高效液相色谱–荧光法的精确度相对较高。
气相色谱–质谱联用法
气相色谱对待测样品进行检测时具有很高的分离能力,而质谱具有灵敏性相对较高和对未知的物质进行定性分析的优点。气相色谱和质谱联用能够扬长避短,使得混合物样品在气相色谱中进行分离后再进入质谱中,能够快速简便的对比较复杂的化合物进行分离,气质联用法也是对苯并芘进行痕量和微量检测分析的重要检测方法之一。例如:李玮等就用此方法对奶粉中的苯并芘进行检测,检测时样品首先用甲醇—氢氧化钾进行皂化,用甲苯进行提取,经过滤膜过滤,测定得出苯并芘的检测限是0.3 ug/kg。
液相色谱–质谱联用法
高效液相色谱–质谱联用法简称LC-MS,是具有很高的分离能力和定性鉴别能力的技术,在检测时能够实现对复杂样品的快速、高效分离。例如:刘玉兰、赵晓涛等用此方法对食用油中苯并芘的含量进行检测,定量时采用内标法对样品的量进行标定,通过气质连用法对样品进行分析得出检测限是0.2~30 ng/ml,检出限是0.1 ng/ml。该检测方法主要适用于样品的精确检测,但是由于它费时比较长,对检测人员的要求比较高,当需要对大批量的样品进行快速检测时,此方法并不适用。[5]

-
芘扎塔娜·翁沙纳塔纳辛
2025-09-27 18:30:32 查看详情 -
苯并异噻唑啉-3-酮
2025-09-27 18:30:32 查看详情


 求购
求购






