- 二氟化二氧

二氟化二氧
物理性质
在熔点以下时,二氟化二氧为黄色晶体。在熔点以上时,二氟化二氧融化成樱红色的油状液体。在沸点以上时为棕色气体。[1]
化学性质
不稳定性
二氟化二氧是一种性质极其不稳定的化合物,即使在-160℃的情况下也能缓慢分解为二氟化氧和氧气。[1]分解速率约为每天4%。按照此规律,完全分解需要25天。二氟化二氧在-57℃以下成为液体并在几分钟之内分解成氟气和氧气。升温使其成为气体时能爆炸式分解。温度越高,二氟化二氧越不稳定。
极强的氧化性
二氟化二氧的氧化性极强,基本和氟原子的氧化性相当。在低于-100℃的极低温度下也能与所有的金属和非金属反应(氦氖氩除外)
二氟化二氧在零下100度,可以与惰性气体氙气、黄金剧烈反应,将氙氧化成六价氙,将金氧化成+5价。[1]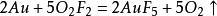
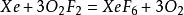
甚至能将一些氟化物中的氟离子氧化,生成氟单质,如三氟化硼,五氟化磷,五氟化砷,四氟化锡,五氟化锑等。[1]
2O2F2+ 2PF5→ 2[O2+]PF6−+ F2
O2F2+ BF3→ [O2+]BF4−+ 1/2 F2
2O2F2+ 2AsF5→2[O2+]AsF6−+F2
以上反应中,氧在反应前后从+1,降低到+1/2,氟的化合价从-1升高到0价。
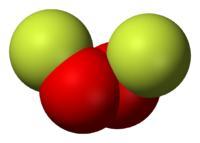 二氟化二氧分子结构需要注意的是O2F2只是将少量的氟化物氧化,并不能将所有的氟化物氧化,比如不能将氟化氢氧化,它的氧化能力应小于等于氟原子,强于氟气。
二氟化二氧分子结构需要注意的是O2F2只是将少量的氟化物氧化,并不能将所有的氟化物氧化,比如不能将氟化氢氧化,它的氧化能力应小于等于氟原子,强于氟气。
制备方法
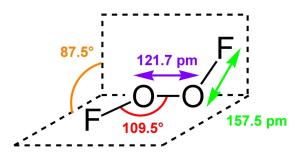 二氟化二氧结构式将以1:1摩尔比混合的氧气和氟气降温到-196℃,气压调节到7-17mmHg,进行辉光放电,即可得到黄色的二氟化二氧晶体。这种化合物于1933年首次制得。
二氟化二氧结构式将以1:1摩尔比混合的氧气和氟气降温到-196℃,气压调节到7-17mmHg,进行辉光放电,即可得到黄色的二氟化二氧晶体。这种化合物于1933年首次制得。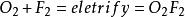
化学用途
用作极强的氧化剂和氟化剂,也用于制取氧正离子盐,还曾经被用来当作液体火箭发动机的氧化剂,但始终未能实用。

-
缩水甘油醚型环氧树脂
2025-09-19 10:40:34 查看详情 -
二氧化碳气体保护焊机
2025-09-19 10:40:34 查看详情


 求购
求购







