- 锑

锑
理化性质
物理性质
锑是一种带有银色光泽的灰色金属,其莫氏硬度为3。因此,纯锑不能用于制造硬的物件:中国的贵州省曾在1931年发行锑制的硬币,但因为锑很容易磨损,在流通过程损失严重。
| 物态 | 固态 |
|---|---|
| 密度 | (接近室温) 6.697g·cm |
| 熔点时液体密度 | 6.53 g·cm |
| 熔点 | 903.78K,630.63°C,1167.13°F |
| 沸点 | 1860K,1587°C,2889°F |
| 熔化热 | 19.79kJ·mol |
| 汽化热 | 193.43 kJ·mol |
| 比热容 | 25.23 J·mol·K |
| 压/Pa | 1 | 10 | 100 | 1 k | 10 k | 100 k |
| 温/K | 807 | 876 | 1011 | 1219 | 1491 | 1858 |
化学性质
| 物态 | 固态 |
|---|---|
| 密度 | (接近室温) 6.697g·cm |
| 熔点时液体密度 | 6.53 g·cm |
| 熔点 | 903.78K,630.63°C,1167.13°F |
| 沸点 | 1860K,1587°C,2889°F |
| 熔化热 | 19.79kJ·mol |
| 汽化热 | 193.43 kJ·mol |
| 比热容 | 25.23 J·mol·K |
化合物
| 压/Pa | 1 | 10 | 100 | 1 k | 10 k | 100 k |
| 温/K | 807 | 876 | 1011 | 1219 | 1491 | 1858 |
化学循环
锑是氮族元素(15族),电负性为2.05。根据元素周期律,它的电负性比锡和铋大,比碲和砷小。锑在室温下的空气中是稳定的,但加热时能与氧气反应生成三氧化二锑。锑在一般条件下不与酸反应。
目前已知锑有四种同素异形体——一种稳定的金属锑和三种亚稳态锑(爆炸性锑、黑锑、黄锑)。金属锑是一种易碎的银白色有光泽的金属。把熔融的锑缓慢冷却,金属锑就会结成三方晶系的晶体,其与砷的灰色同素异形体异质同晶。罕见的爆炸性锑可由电解三氯化锑制得,用尖锐的器具刮擦它就会发生放热的化学反应,放出白烟并生成金属锑。如果在研钵中用研杵将它磨碎,就会发生剧烈的爆炸。黑锑是由金属锑的蒸汽急剧冷却形成的,它的晶体结构与红磷和黑砷相同,在氧气中易被氧化甚至自燃。当温度降到100℃时,它逐渐转变成稳定的晶型。黄锑是最不稳定的一种,只能由锑化氢在-90℃下氧化而得。在这种温度和环境光线的作用下,亚稳态的同素异形体会转化成更稳定的黑锑。[3]
 金属锑的结构为层状结构(空间群:R3m No. 166),而每层都包含相连的褶皱六元环结构。最近的和次近的锑原子形成变形八面体,在相同双层中的三个锑原子比其他三个相距略近一些。这种距离上的相对近使得金属锑的密度达到6.697g/cm,但层与层之间的成键很弱也造成它很软且易碎。
金属锑的结构为层状结构(空间群:R3m No. 166),而每层都包含相连的褶皱六元环结构。最近的和次近的锑原子形成变形八面体,在相同双层中的三个锑原子比其他三个相距略近一些。这种距离上的相对近使得金属锑的密度达到6.697g/cm,但层与层之间的成键很弱也造成它很软且易碎。
同位素
锑有两种稳定同位素,Sb的自然丰度为57.36%,而Sb的自然丰度为42.64%。锑还有35种放射性同位素,其中半衰期最长的Sb为2.75年。此外,目前已发现了29种亚稳态。这其中最稳定的是Sb,半衰期为60.20天,它可以用作中子源。比稳定同位素Sb轻的同位素倾向于发生β衰变,而较重的同位素更易发生β衰变。当然也有一些例外。
生产
锑化合物通常分为+3价和+5价两类。与同主族的砷一样,它的+5氧化态更为稳定。
氧化物与氢氧化物
三氧化二锑可由锑在空气中燃烧制得。在气相中,它以双聚体Sb4O6的形式存在,但冷凝时会形成多聚体。五氧化二锑只能用浓硝酸氧化三价锑化合物制得。锑也能形成混合价态化合物——四氧化二锑,其中的锑为Sb(III)和Sb(V)。与磷和砷不同的是,这些氧化物都是两性的,它们不形成定义明确的含氧酸,而是与酸反应形成锑盐。
目前还没有制得亚锑酸(Sb(OH)3),但它的共轭碱亚锑酸钠([Na3SbO3]4)可由熔融的氧化钠与三氧化二锑反应制得。过渡金属的亚锑酸盐也已制得。锑酸只能以水合物HSb(OH)6的形式存在,它形成的盐中含有Sb(OH)−6。这些盐脱水得到混合氧化物。
许多锑矿石是硫化物,其中如辉锑矿(Sb2S3)、深红银矿(Ag3SbS3)、辉锑铅矿、脆硫锑铅矿和硫锑铅矿。五硫化二锑是一种非整比化合物,锑处于+3氧化态并含有S-S键。有多种硫代锑酸盐是已知的,例如[Sb6S10]和[Sb8S13]。
卤化物
锑能形成两类卤化物——SbX3和SbX5。其中三卤化物(SbF3、SbCl3、SbBr3和SbI3)的空间构型都是三角锥形。三氟化锑可以由三氧化二锑与氢氟酸反应制得:
- Sb2O3+ 6HF → 2SbF3+ 3H2O
这种氟化物是路易斯酸,能结合氟离子形成配离子SbF4⁻和SbF5²⁻。熔化的三氟化锑是一种弱的导体。三氯化锑则由三硫化二锑溶于盐酸制得:
- Sb2S3+ 6HCl → 2SbCl3+ 3H2S
 五卤化物(SbF5和SbCl5)气态时的空间构型为三角双锥形。但是转化为液态后,五氟化锑形成聚合物,而五氯化锑依旧是单体。五氟化锑是很强的路易斯酸,可用于配制著名的超强酸氟锑酸(HSbF6)。
五卤化物(SbF5和SbCl5)气态时的空间构型为三角双锥形。但是转化为液态后,五氟化锑形成聚合物,而五氯化锑依旧是单体。五氟化锑是很强的路易斯酸,可用于配制著名的超强酸氟锑酸(HSbF6)。
锑的卤氧化物比砷和磷更为常见。三氧化二锑溶于浓酸再稀释可形成锑酰化合物,例如SbOCl和(SbO)2SO4。
锑化物、氢化物与有机锑化合物
这类化合物通常被视作Sb的衍生物。Sb金属性不强,能与金属形成锑化物,例如锑化铟(InSb),锑化银(Ag3Sb),锑钯矿(Pd5Sb2),方锑金矿(AuSb2),红锑镍矿(NiSb)等。碱金属和锌的锑化物,例如Na3Sb和Zn3Sb2比以上物质更为活泼。这些锑化物用酸处理可以生成不稳定的气体锑化氢(SbH3)。
锑化物一般以共价键链接,是电子云的重叠,所以共价键最本质的分类方式就是它们的重叠方式。σ键,π键,δ键在有机化合物中,通常把共价键以其共用的电子对数分为单键、双键以及三键。单键是一根σ键;双键和三键都含一根σ键,其余1根或2根是π键。但无机锑化物不用此法。原因是,无机锑化物中经常出现的共轭体系(离域π键)使得某两个原子之间共用的电子对数很难确定,因此无机物中常取平均键级,作为键能的粗略标准。
- Sb³⁻+3H⁺=SbH3↑
有机锑化合物一般可由格氏试剂对卤化锑的烷基化反应制备。已知有大量三价和五价的有机锑化合物——包括混合氯代衍生物,还有以锑为中心的阳离子和阴离子。例如Sb(C6H5)3(三苯基锑)、Sb2(C6H5)4(含有一根Sb-Sb键)以及环状的[Sb(C6H5)]n。五配位的有机锑化合物也很常见,例如Sb(C6H5)5和一些类似的卤代物。
历史
锑是全球性污染物,是目前国际上最为关注的有毒金属元素之一。与其它有毒金属如汞和砷等相比,人们对锑的环境污染过程和生物地球化学循环还缺乏系统认识。
化学形态、微生物和有机质的影响,及同位素等现代分析技术是目前研究锑生物地球化学循环强有力的研究手段,可以为某些关键重要的环节提供新的思路,在此基础上,建立地表环境中锑的生物地球化学演化、归宿以及与人体健康的关系的基本认识框架,为其它类型锑污染咖城市地表环境)的评价和治理提供借鉴。
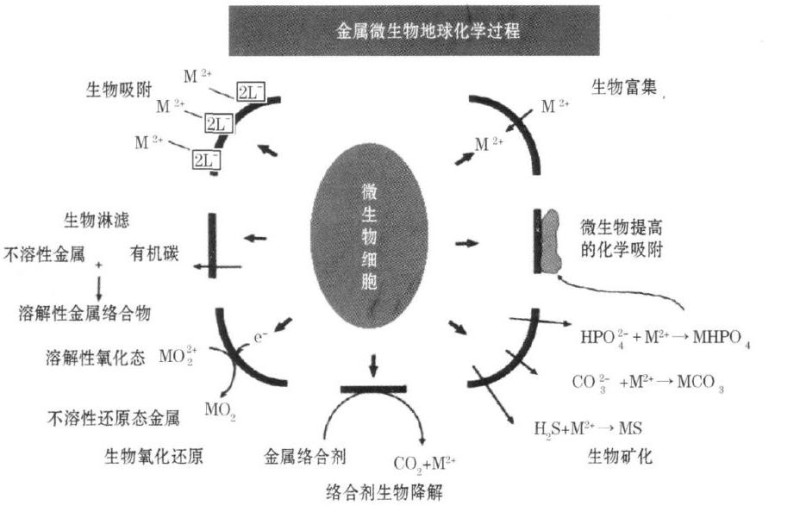
有机质和(微)生物的影响
近些年的研究表明生物活动和有机质参与了环境中锑的迁移转化等。生物对锑的吸收和吸附过程取决于锑的形态和微环境如微生物,溶解三价锑很容易被植物根系吸收,而五价锑则很难被吸收。
大量最新的研究结果表明:天然有机质对微量金属元素如汞、铜、铅、钻和铁等的生物地球化学循环过程起着十分重要的作用,这是由于有机质能与金属离子形成有机金属配位体,导致金属元素生物地球化学行为的改变,影响其溶解性、生物有效性、与微粒之间的相互作用并改变它们的毒性。
因此,金属与有机质的相互作用机理是近年来环境化学领域注目的焦点。由于目前关于锑与有机质相互作用的研究相对较少,有机质对锑生物地球化学循环的影响程度和机理还不清楚。但从目前相关的文献报道可以看出:在水环境中,有机结合态锑占总锑相当大的份额,在海水和湖水中,锑与有机质结合比例可高达;土壤和沉积物中有机质结合态锑占总锑的比例还不清楚,预计会比水体中更大。
同位素示踪
近几年来,由于MC-ICP-MS的发展以及高效率离子化氢等离子体的出现,准确和高精度的同位素比值测定成为可能,一些金属如铜、铁、锌、铂和硒等稳定同位素系统的研究已为认识这些金属的生物地球化学过程和自然分馏研究提供了一种全新的技术手段。因此,金属元素的稳定同位素研究是目前金属元素环境与生物地球化学领域的前沿领域之一。同位素为锑在地表环境的无机与生物过程示踪和来源研究提供了全新的技术手段。
应用
生产国
根据英国地质调查局2005年的报告,中华人民共和国是世界上锑产量最大的国家,占了全球的84%,远远超出其后的南非、玻利维亚和塔吉克斯坦。湖南省冷水江市的锡矿山是世界最大锑矿,估计储量为210万吨。
2010年,根据美国地质调查局的报告,中国生产的锑占全球的88.9%。[4]
| 国家 | 产量(吨) | 占比(%) |
|---|---|---|
| 中华人民共和国 | 120,000 | 88.9 |
| 南非 | 3,000 | 2.2 |
| 玻利维亚 | 3,000 | 2.2 |
| 俄罗斯 | 3,000 | 2.2 |
| 塔吉克斯坦 | 2,000 | 1.5 |
| 其他国家 | 4,000 | 3.0 |
| 全球 | 135,000 | 100.0 |
然而,英国洛斯基矿业咨询公式估计2010年中华人民共和国的初级生产锑产量占全球的76.75%(全球合计120,462吨,其中90,000吨是公开报道的,30,462吨未报道),紧接着的是俄罗斯(占4.14%,产量6,500吨)、缅甸(占3.76%,产量5,897吨)、加拿大(占3.61%,产量5,660吨)、塔吉克斯坦(占3.42%,产量5,370吨)和玻利维亚(占3.17%,4,980吨)。
洛斯基公司估计全球在2010年的次级生产锑产量为39,540吨。
英国地质调查局在2011年下半年将锑列在风险列表第一位。这个列表表示如果化学元素不能稳定供应,会对维持英国经济和生活方式造成的相对风险。根据洛斯基公司的报告,2014年中国的锑产量有所减少,并且在未来一段时间不可能上升。中国已没有开发十年左右的重要锑矿床,这种重要的经济储备资源将迅速枯竭。
同时,欧盟在2011年的一份报告中也将锑列为12种关键的原料之一,主要是因为来自中国以外的锑产量很少。
以下是洛斯基公司提供的2014年世界锑的主要生产者:
| 国家 | 公司 | 产量(吨/年) |
|---|---|---|
| 中国 | 闪锑度矿业(前锡矿山闪星锑业) | 2,750 |
| 玻利维亚 | 许多 | 5,460 |
| 加拿大 | 比弗·布鲁克 | 6,000 |
| 中国 | 布鲁克投资集团 | 55,000 |
| 中国 | 湖南辰州矿业 | 20,000 |
| 中国 | 华锡集团 | 20,000 |
| 中国 | 沈阳华昌锑业 | 15,000 |
| 哈萨克斯坦 | Kazzinc | 1,000 |
| 吉尔吉斯斯坦 | Kadamdzhai | 500 |
| 老挝 | SRS | 500 |
| 墨西哥 | 美国锑业 | 70 |
| 缅甸 | 许多 | 6,000 |
| 俄罗斯 | GeoPDroMining | 6,500 |
| 南非 | 默奇森联合公司 | 6,000 |
| 塔吉克斯坦 | YUnzob | 5,500 |
| 泰国 | 未知 | 600 |
储量
根据美国地质调查局的统计数据,世界的锑矿藏将在13年内枯竭。但美国地质调查局期待这期间会发现更多锑矿。
| 国家 | 储量(吨) | 占比(%) |
|---|---|---|
| 中华人民共和国 | 950,000 | 51.88 |
| 俄罗斯 | 350,000 | 19.12 |
| 玻利维亚 | 310,000 | 16.93 |
| 塔吉克斯坦 | 50,000 | 2.73 |
| 南非 | 21,000 | 1.15 |
| 其他国家 | 150,000 | 8.19 |
| 全球 | 1,831,000 | 100.0 |
生产过程
从矿石中提取锑的方法取决于矿石的质量与成分。大部分锑以硫化物矿石形式存在。低品位矿石可用泡沫浮选的方法富集,而高品位矿石加热到500–600℃使辉锑矿熔化,并得以从脉石中分离出来。锑可以用铁屑从天然硫化锑中还原并分离出来:
- Sb2S3+ 3Fe → 2Sb + 3FeS
三硫化二锑比三氧化二锑稳定,因此易于转化,而焙烧后又恢复成硫化物。这种材料直接用于许多应用中,可能产生的杂质是砷和硫化物。 将锑从氧化物中提取出来可使用碳的热还原法:
- 2Sb2O3+ 3C → 4Sb + 3CO2
低品味的矿石在高炉中还原,而高品味的则在反射炉中还原。
阻燃剂
| 国家 | 产量(吨) | 占比(%) |
|---|---|---|
| 中华人民共和国 | 120,000 | 88.9 |
| 南非 | 3,000 | 2.2 |
| 玻利维亚 | 3,000 | 2.2 |
| 俄罗斯 | 3,000 | 2.2 |
| 塔吉克斯坦 | 2,000 | 1.5 |
| 其他国家 | 4,000 | 3.0 |
| 全球 | 135,000 | 100.0 |
合金
| 国家 | 公司 | 产量(吨/年) |
|---|---|---|
| 中国 | 闪锑度矿业(前锡矿山闪星锑业) | 2,750 |
| 玻利维亚 | 许多 | 5,460 |
| 加拿大 | 比弗·布鲁克 | 6,000 |
| 中国 | 布鲁克投资集团 | 55,000 |
| 中国 | 湖南辰州矿业 | 20,000 |
| 中国 | 华锡集团 | 20,000 |
| 中国 | 沈阳华昌锑业 | 15,000 |
| 哈萨克斯坦 | Kazzinc | 1,000 |
| 吉尔吉斯斯坦 | Kadamdzhai | 500 |
| 老挝 | SRS | 500 |
| 墨西哥 | 美国锑业 | 70 |
| 缅甸 | 许多 | 6,000 |
| 俄罗斯 | GeoPDroMining | 6,500 |
| 南非 | 默奇森联合公司 | 6,000 |
| 塔吉克斯坦 | YUnzob | 5,500 |
| 泰国 | 未知 | 600 |
其他应用
| 国家 | 储量(吨) | 占比(%) |
|---|---|---|
| 中华人民共和国 | 950,000 | 51.88 |
| 俄罗斯 | 350,000 | 19.12 |
| 玻利维亚 | 310,000 | 16.93 |
| 塔吉克斯坦 | 50,000 | 2.73 |
| 南非 | 21,000 | 1.15 |
| 其他国家 | 150,000 | 8.19 |
| 全球 | 1,831,000 | 100.0 |
安全
锑的一种炼金术符号为♀形
早在公元前3100年的埃及前王朝时代,化妆品刚被发明,三硫化二锑就用作化妆用的眼影粉。
在迦勒底的泰洛赫(今伊拉克),曾发现一块可追溯到公元前3000年的锑制史前花瓶碎片;而在埃及发现了公元前2500年至前2,200年间的镀锑的铜器。奥斯汀在1892年赫伯特·格拉斯顿的一场演讲时说道:“我们只知道锑现在是一种很易碎的金属,很难被塑造成实用的花瓶,因此这项值得一提的发现(即上文的花瓶碎片)表现了已失传的使锑具有可塑性的方法。”然而,默里(Moorey)不相信那个碎片真的来自花瓶,在1975年发表他的分析论文后,认为斯里米卡哈诺夫(Selimkhanov)试图将那块金属与外高加索的天然锑联系起来,但用那种材料制成的都是小饰物。这大大削弱了锑在古代技术下具有可塑性这种说法的可信度。
欧洲人万诺乔·比林古乔于1540年最早在《火焰学》(De la pirotechnia)中描述了提炼锑的方法,这早于1556年阿格里科拉出版的名作《论矿冶》(De re Metallica)。此书中阿格里科拉错误地记入了金属锑的发现。1604年,德国出版了一本名为《Currus Triumphalis Antimonii》(直译为“凯旋战车锑”)的书,其中介绍了金属锑的制备。15世纪时,据说笔名叫巴西利厄斯·华伦提努的圣本笃修会的修士提到了锑的制法,如果此事属实,就早于比林古乔。
一般认为,纯锑是由贾比尔(Jābir ibn Hayyān)于8世纪时最早制得的。然而争议依旧不断,翻译家马塞兰·贝特洛声称贾比尔的书里没有提到锑,但其他人认为贝特洛只翻译了一些不重要的著作,而最相关的那些(可能描述了锑)还没翻译,它们的内容至今还是未知的。
地壳中自然存在的纯锑最早是由瑞典籍英国科学家威廉·亨利·布拉格于1783年记载的。品种样本采集自瑞典西曼兰省萨拉市的萨拉银矿。
词条图册
60%的锑用于生产阻燃剂,而20%的锑用于制造电池中的合金材料、滑动轴承和焊接剂。



 求购
求购









