- 胰岛移植

胰岛移植
病因
引起胰岛移植的原因主要为人类胰腺B细胞;其他动物胰腺,例如猪;诱导人胰腺导管细胞;诱导胎儿胰腺干细胞;治疗克隆技术生产的B细胞自体移植。
症状
 通过多例临床资料已经证明,对伴有感知障碍性低血糖的1型DM,胰岛移植确实能起到稳定血糖,缓解低血糖发作,挽救生命的作用。80%的1型DM在移植后可检测到血C-肽,但长期随访发现达到胰岛素非依赖的比例低,仅占10%左右,且维持时间短,平均脱离胰岛素的期限为15个月。在观察指标中,成功移植者HbA1c显著改善,低血糖分数和血糖波动指数明显好转。有意义的研究发现,移植后胰高糖素的反应性亦明显提高。此外,移植成败并不加重胰岛素抵抗程度。
通过多例临床资料已经证明,对伴有感知障碍性低血糖的1型DM,胰岛移植确实能起到稳定血糖,缓解低血糖发作,挽救生命的作用。80%的1型DM在移植后可检测到血C-肽,但长期随访发现达到胰岛素非依赖的比例低,仅占10%左右,且维持时间短,平均脱离胰岛素的期限为15个月。在观察指标中,成功移植者HbA1c显著改善,低血糖分数和血糖波动指数明显好转。有意义的研究发现,移植后胰高糖素的反应性亦明显提高。此外,移植成败并不加重胰岛素抵抗程度。
检查
胰岛移植的检查主要为胰岛分离后的培养温度、胰岛培养天数及保存方法、免疫抑制剂及血糖。
诊断
从结构和功能上来讲,胰腺是兼有外分泌和内分泌功能的腺体,其外分泌部分,主要消化进入体内的食物;其内分泌部分由胰岛组成,胰岛虽小但也是一个复杂的组织(胰岛只是一种组织,而非器官),胰岛素分泌受损将会导致糖尿病发生。胰腺移植是将供者胰腺通过外科手术移植到受者体内;胰岛移植技术是将通过体外一系列处理后的胰岛,经穿刺、注射、介入等方法移植到受者体内。
治疗
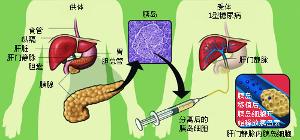 糖尿病已经成为全球性、发病率逐渐增加性疾病。外源性补充胰岛素及口服降糖药是治疗糖尿病的主要手段,建立内源性胰岛素分泌系统是人们一直在研究的热点。胰岛移植是较胰腺移植更具有简单、安全、有效、副作用小等优点。胰岛移植的方法有以下几种:
糖尿病已经成为全球性、发病率逐渐增加性疾病。外源性补充胰岛素及口服降糖药是治疗糖尿病的主要手段,建立内源性胰岛素分泌系统是人们一直在研究的热点。胰岛移植是较胰腺移植更具有简单、安全、有效、副作用小等优点。胰岛移植的方法有以下几种:
同种胰岛移植
1.1自体胰岛移植 主要用于慢性胰腺炎及胰腺癌术后。自体移植可避免排斥反应,多数能获得成功。最主要的影响因素是自体胰岛细胞数量有限,影响远期疗效。
1.2 异体移植
1.2.1 成人胰岛移植 成人胰岛来源相对比较充足,但因其免疫原性较强,易产生强烈排斥反应,另外成人胰岛对缺氧耐受力较弱,胰腺外分泌较强,因而受到限制。采用雷帕霉素、FK-506和人源化白介素-2(IL-2)受体抗体取得了较好疗效,从而避免了类固醇激素对胰岛细胞的毒性及对机体的代谢紊乱。此方案要求有2~3个成人胰供体,可使受体得到相对多的存活胰岛。此方案远期效果如何有待进一步观察。
1.2.2 胎儿胰岛移植 胎儿胰岛移植具有:(1)外分泌组织发育不成熟,抗原性较弱;(2)胰岛组织丰富,内分泌成分含量高;(3)胰岛细胞增殖能力强,再生能力亦强;(4)对低温、缺氧耐受力好,便于保存等优点。同时,胎儿胰岛移植又有胰岛移植物数量不足、移植后基础C肽恢复不理想及胎儿胰岛在体外高浓度葡萄糖刺激下胰岛素分泌不足等缺点,因而一次移植难以取得满意效果。
异种胰岛移植
猪胰岛:猪胰岛与人胰岛仅有1个氨基酸差别且来源比较容易,因而是最有希望成为临床异种移植的供体。猪供胰可分为胎儿猪及成年猪两种:胎猪免疫原性弱,但体外培养对糖刺激反应较差;成年猪胰岛数量较多,对糖刺激应答较好,但免疫原性强。目前用于人胰腺的消化、分离和纯化胰岛的方法不适用于猪胰岛的提取,因而效率低,胰岛死亡率高,这些使得猪胰岛移植的应用增加了很多困难。新生猪胰腺组织内有大量胰岛干细胞,具有潜在的生长、分化能力,因此目前许多研究集中于胚胎或新生猪胰岛组织。
胰岛细胞株
尽管胰岛β细胞有一定的生长能力,但目前尚无体外扩增β细胞的可行方法。
干细胞
干细胞根据其分化潜能分为全能干细胞、多能干细胞和定向干细胞;根据个体发育过程中出现的先后次序不同,又分为胚胎干细胞和成体干细胞。可能用于诱导分化成为胰岛的干细胞包括胚胎干细胞、胚胎生殖细胞等全能干细胞;成体干细胞中的间质干细胞(肝、骨髓、胰腺)、肠上皮细胞等多能干细胞及胰腺导管细胞等定向干细胞 。
并发症
虽然胰岛移植的疗效有了很大提高,但是移植和免疫抑制相关的并发症和副作用也比原先估计的要多。与雷帕霉素相关的副作用有口腔溃疡、腹泻、水肿、体重减轻、 血脂升高、痤疮、月经紊乱、卵巢囊肿、骨髓抑制(贫血、中性粒细胞减少、血小板减少)和肺炎等,与他克莫司相关的副作用有肾功能恶化、高血压、震颤以及体 内的胰岛毒性作用等,与操作相关的副作用有腹腔出血、门静脉血栓形成、转氨酶暂时升高、脂肪肝等。部分患者因严重副作用而停用免疫抑制剂。[1]

-
胰岛素泵规范治疗教程
2025-11-02 22:37:42 查看详情 -
常规重组人胰岛素注射液
2025-11-02 22:37:42 查看详情 -
抗胰岛细胞抗体(ICA)
2025-11-02 22:37:42 查看详情


 求购
求购






