- 泌乳素瘤

泌乳素瘤
疾病描述
泌乳素瘤(prolactinoma)是常见的下丘脑-垂体疾病。泌乳素瘤是高泌乳素血症最常见的病因,女性居多,男性少见。在垂体腺瘤中泌乳素瘤占50%~55%。120例生前并无垂体疾病症状的尸检报告发现27%的人有垂体微腺瘤,无年龄、性别差异。
虽然生前大多数人并无内分泌紊乱的表现,但这些微腺瘤经免疫组化分析表明有41%属泌乳素瘤。临床上有症状的泌乳素微腺瘤一般不会长成大腺瘤,血泌乳素(PRL)浓度升高也不明显,甚至可以下降。部分腺瘤有侵袭性,以后出现腺瘤增大及血PRL增高。
症状体征
女性表现为溢乳、闭经(血PRL>50ug/L、特发性高催乳素血症者月经正常),不育与性功能减退、青少年发病者发育延迟,还可有多毛和痤疮、骨质疏松、肥胖、水潴留。男性症状少,主要是阳萎,不育,少数有溢乳、乳房发育、毛发稀,多因垂体腺瘤出现压迫症状而就医。
疾病病因
1.病理性高PRL血症病理性高PRL血症多见于下丘脑-垂体疾病,以PRL瘤最为多见。除PRL瘤(或含有PRL瘤的混合瘤)外,其他下丘脑-垂体肿瘤、浸润性或炎症性疾病、结节病、肉芽
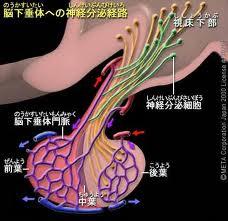 泌乳素瘤肿以及外伤、放射性损伤等均是由于下丘脑多巴胺生成障碍或阻断垂体门脉血流致使多巴胺等泌乳素释放抑制因子(PIF)不能到达腺垂体所致。由于泌乳素释放因子(PRF)增多引起高PRL血症的情况见于原发性甲减、应激刺激和神经源性刺激。慢性肾功能衰竭患者由于肾小球滤过清除PRL障碍而导致高PRL血症。肝硬化患者由于雌激素和PRL在肝脏的灭活障碍致血PRL升高。某些风湿性疾病如系统性红斑狼疮(SLE)、干燥综合征、系统性硬化症也可出现高PRL血症,但与疾病的活动性和血清学异常无相关性,自身免疫性疾病伴高PRL血症的原因不明。高泌乳素血症可伴或不伴溢乳。
泌乳素瘤肿以及外伤、放射性损伤等均是由于下丘脑多巴胺生成障碍或阻断垂体门脉血流致使多巴胺等泌乳素释放抑制因子(PIF)不能到达腺垂体所致。由于泌乳素释放因子(PRF)增多引起高PRL血症的情况见于原发性甲减、应激刺激和神经源性刺激。慢性肾功能衰竭患者由于肾小球滤过清除PRL障碍而导致高PRL血症。肝硬化患者由于雌激素和PRL在肝脏的灭活障碍致血PRL升高。某些风湿性疾病如系统性红斑狼疮(SLE)、干燥综合征、系统性硬化症也可出现高PRL血症,但与疾病的活动性和血清学异常无相关性,自身免疫性疾病伴高PRL血症的原因不明。高泌乳素血症可伴或不伴溢乳。
2.药物性高PRL血症能引起高PRL血症的药物众多,包括多巴胺受体拮抗剂、含雌激素的口服避孕药、某些抗高血压药、阿片制剂及H2受体阻滞剂(如西咪替丁)等。其中多巴胺受体拮抗剂是一些具有安定、镇静或镇吐作用以及抗抑郁、抗精神病类药物。在常用剂量时血PRL一般不超过100μg/L。口服多潘立酮5~7天后所致高PRL血症水平在35~70μg/L之间,偶可明显升高,被误诊为PRL瘤。由于氯丙嗪和甲氧氯普胺(胃复安)的作用最强,25mg氯丙嗪可使正常人血清PRL水平增加5~7倍,故常用于PRL的动态试验以协助PRL瘤的诊断。
3.PRL瘤PRL瘤的发病机制曾有过几种假说。以往认为长期服用雌激素可能是PRL瘤形成的原因,但大规模研究表明口服避孕药,尤其是低剂量的雌激素和PRL瘤的形成并无联系。现认为垂体的自身缺陷是PRL瘤形成的起始原因,下丘脑调节功能紊乱仅起着允许和促进作用。用分子生物学技术在人类腺垂体肿瘤中找到一些候选基因,其中与PRL瘤有关的肿瘤激活基因有肝素结合分泌性转型基因(heparin binding secretory transforming gene,HST)、垂体瘤转型基因(pituitary tumor transforming gene,PTTG)。
肿瘤抑制基因有CDKN2A基因和MENI基因,后者在家族性多发性内分泌腺瘤综合征-I型患者中被发现。由于这些基因的变异,解除了垂体干细胞的生长抑制状态,转化成某种或几种腺垂体细胞,并发生单克隆增殖。在下丘脑激素调节紊乱、腺垂体内局部形成肿瘤,导致某种或几种腺垂体激素自主性合成和分泌。特异性肿瘤分子标志物的发现有助于微腺瘤的早期诊断及治疗,并为选择合适的随访方案提供依据,对家族性MEN-I进行家族筛查也将成为可能。
诊断检查
1.临床特征
(1)闭经,早期可有月经过多或不规则。
(2)溢乳,约占50%女性患者。
(3)两性均可有不孕(育)和不同程度的性功能减退。
(4)垂体瘤占位压迫的临床症状与体征,如头痛、视野缺损和视力减退等。
(5)除外某些药物因素。
2.辅助检查
(1)血PRL测定:正常人空腹血清PRL小于20μg/L,泌乳素瘤患者血清PRL多大于100μg/L,大于300μg/L几乎可以肯定存在泌乳素瘤。
(2)蝶鞍正、侧位片垂体CT或磁共振检查:可证实肿瘤的存在。视野检查可协助诊断。
(3)血清FSH、LH、雌二醇(E2)值均可减低。
(4)必要时可作TRH兴奋试验、甲氧氯普胺试验,对诊断泌乳素瘤有一定的参考价值。
(5)作相关检查,以排除原发性甲状腺功能减退和下丘脑、垂体及其他内分泌疾病,除外脑部、乳房疾患。
检查化验
一、PRL >100ug/L者高度考虑泌乳素瘤;> 200ug/L绝大多数为泌乳素瘤;RL<100ug/L者多考虑高泌乳素血症.PRL抑制试验 口服L-多巴500mg,于服药前及服药后1、2、3及6h测PRL。正常服药后1-3hPRL 水平抑制到4ug/L以下或基础值的50%以上, 以后逐渐回升,泌乳素瘤患者不被抑制。
二、TRH兴奋试验 基础状态下静注TRH200ug,于注射前30min,注射后15、30、60、120及180min分别测PRL。正常及高泌乳素血症患者峰值大多出现在注射后30min,峰/基比值>2,泌乳素瘤患者峰值出现延迟,峰/基比<1.5。
三、灭吐灵兴奋试验 服灭吐灵前及服药后1、2及3h 分别测PRL。正常及高泌乳素血症患者峰值在1-2h,峰/基比值>3。泌乳素瘤患者峰/基比值<1.5。
四、其他激素检测;促性腺激素正常或偏低,对GnRH兴奋试验呈增强反应;女性患者雌二醇低下;男性睾酮降低。
五、影像学检查:蝶鞍X片大多正常。垂体CT扫描或MRI可发现微腺瘤。 [1]
其他辅助检查
对所有病理性高PRL血症患者,在怀疑为下丘脑-垂体疾病而做X线、CT或MRI检查前,必须首先详细询问病史、体格检查及常规肝、肾功能检查并逐一排除药物性、应激性、神经源性及系统性疾病可能,其中尤其要排除原发性甲状腺功能减低症。
1.蝶鞍区X线平片由于PRL瘤微腺瘤多见,常规X线平片多不能发现蝶鞍扩大
或侵蚀。垂体瘤增大到一定程度可造成蝶鞍骨质局部破坏的X线表现(如鞍区扩大,骨质变薄或缺损等)。由此可推测垂体瘤的存在,但无法确定肿瘤大小,更无法发现垂体微腺瘤。正常鞍结节角约为110°,随着PRL瘤增大,此角可渐变为锐角,据此也可推断垂体瘤的存在。做气脑造影或脑动脉X线显影检查虽然在一定程度上可以显示垂体瘤的大小等,但是属有创性检查且伴有一定的风险。己被CT和MRI的普及应用所替代。
此外薄分层(2mm)多层断层X线摄片中的鞍底阳性征象,正位显示鞍底倾斜,侧位显示鞍底前下壁起泡状膨胀伴鞍结节角缩小,这两点可作为PRL瘤的X线重要特征,其诊断价值远较平片为高。根据Guiot和Hardy的标准,将垂体微腺瘤的放射学表现分为局限型与侵蚀型。
2.蝶鞍区CT及MRI检查是否存在垂体瘤,蝶鞍CT扫描和MRI显像是目前普遍使用的影像检查方法,尤其MRI优于CT而应用更多。
(1)CT检查:CT扫描克服了大多数常规X线方法的限制,只需较小的X线辐射量和可以直接观察垂体肿瘤的影像。采用高分辨率直接冠状位连续薄分层并矢状重建扫描法,同时静脉注射不透X线的含碘对比剂增强扫描,不仅能直接清楚地观察垂体大腺瘤,还可能发现3~4mm的微小腺瘤,用于治疗后复查准确率高。CT扫描正常成人脑垂体高度,女性<8mm、男性<7mm,密度均匀,上缘稍凹陷,垂体柄居中、左右对称。CT扫描垂体瘤的阳性所见为:
①未注射造影对比剂(平扫)时,有隐约可见的高密度区。
②注射造影剂后,见鞍区腺垂体组织影像增强、高度超过正常、垂体柄移位。
③垂体腺形态异常、增大、上缘膨隆、两侧不对称,大腺瘤时可向鞍上、鞍旁扩展,占据鞍上池、第三脑室、海绵窦等。
④非增强或增强扫描时,腺体密度不匀,有低密度区,在微腺瘤时低密度区直径达垂体腺的1/2或更大。
⑤鞍底骨质倾斜、破坏。
CT扫描有其局限性,对鞍内微腺瘤假阳性和假阴性仍然较高。Swartz等报道,正常生育年龄女性垂体上缘也可以有隆起、密度不均匀和局部低密度区。有报道手术证实为微腺瘤的病例,CT检出率是85%。对鞍区的囊性肿物和空泡蝶鞍(emptysella)的鉴别有困难时,可用水溶性的甲泛葡胺(metrizamide)做脑池造影CT扫描,以得到明确的诊断。
(2)MRI检查:MRI检查比CT扫描更灵敏、更具有特异性。MRI在
诊断下丘脑-垂体疾病尤其是垂体瘤时优于CT。虽然MRI和高分辨率CT(冠状位多薄层矢状重建扫描)可发现直径小于3mm的微小腺瘤。但MRI可更好地观察垂体瘤内部结构及其与周围组织的关系,了解病变是否侵犯视交叉、颈静脉窦、蝶窦以及侵犯程度,对纤细的垂体柄是否断裂或被占位病灶压迫等细微变化的观察效果也优于CT。
垂体微腺瘤的MRIT1加权像表现为圆形的低密度影,T2加权像的密度更高些。大腺瘤的影像片类似于正常腺组织,但其内可出现囊性变及出血灶。当怀疑垂体有PRL微腺时,可用Gd-DPTA作增强剂进行冠状位MRI增强扫描,以增加微小腺瘤发现的几率。MRI还可发现一些非垂体性的鞍内占位病变(如脑膜瘤及颈内动脉瘤)。用MRI诊断PRL微腺瘤时,垂体凸出度的诊断价值不及垂体高度。另外,MRI不能显示骨质的破坏及钙化组织。
3.放射性核素检查用111In-pentertreotide行垂体瘤显像,在生长激素分泌瘤及无功能大腺瘤较满意。对PRL瘤,尤其是微腺瘤及手术后残余瘤显像的价值有待进一步研究。
鉴别诊断
应区分其他病因所致的高泌乳素血症
1、生理因素如妊娠、产后、乳头刺激、新生儿、月经中期(因雌激素增高)、睡眠、性交等;
2、病理因素:其他垂体肿瘤;下丘脑疾病;空蝶鞍综合征;异位泌乳素瘤;原发性甲状腺切能减退症;肾功能衰竭;胸部及乳房疾病。
3、 药物:如雌激素的避孕药;吗啡及催眠药;三环类抗郁剂、利血平和氯丙嗪类; 抗多巴胺药物;酚噻嗪、异烟肼、 异搏停、赛庚啶、甲氰咪胍等;
4.特发性高泌乳素血症。
并发症
常导致高泌乳素血症。
治疗方案
泌乳素瘤的治疗,决定于瘤体大小、PRL增高的水平、症状及生育要求。
一、药物治疗:
首选溴隐亭,开始睡前1.25mg,每隔2-3天增加1.25-2.5mg,每日有效量为5-7.5mg。治疗后血PRL下降,2-3月后月经来潮。用药1年左右可停药观察,但复发率逐年增高。
二、手术治疗:
适用于①溴隐亭治疗3 月以上无明显效果的巨大腺瘤,②要求生育的患者,但手术治疗往往不彻底,术后大多仍须溴隐亭治疗。
三、放射治疗:
可防止停药后复发,以求长期控制。
四、妊娠期泌乳素瘤的处理:
1、妊娠期使泌乳素瘤增大的危险性很小。
2、一旦受孕应立即停用溴隐亭;
3、下述情况应引产或再服用溴隐亭:瘤体>10mm,每4-6周检查视野,如出现头痛、视野缩小者应予以引产。如必须推迟分娩, 则应持续应用溴隐亭使瘤体缩小。
4、用溴隐亭的孕妇产后24小时一般宜停药。 产后不宜哺乳。
5、产褥期使用溴隐亭的患者应注意避孕剂的影响,若需避孕,不宜使用雌激素类避孕药。[2]
预后及预防
1.凡有临床症状的病人应该用药物治疗,纠正高泌乳素血症,抑制泌乳,恢复月经,预防可能形成的腺瘤或瘤体增大,预防或减轻骨质疏松,应定期随访。
2.停用引起PRL水平升高的各种药物。



 求购
求购









