- 顺铂

顺铂
基本简介
基本信息
中文名称:顺铂
中文别名:顺二氯二氨基铂;顺双氯双氨络铂;顺-二氯二氨合铂;顺-双氯双氨络铂;顺氯氨铂;顺-二胺二氯铂(II);(Z)-二氨二氯铂;顺式-二胺二氯铂;
英文名称:cisplatin
英文别名:cis-Dichlorodiammine platinum(II);cis-Dichlorodiamineplatinum(II);cis-Diamminedichloroplatinum(II);cis-Diammineplatinum(II) dichloride;cis-Platinum(II) diammine dichloride;cis-Diamineplatinum(II) dichloride;cis-Diammineplatinum dichloride;Cisplatin;cis-Diammineplatinum(II) dichloride (cis-Dichlorodiammine platinum(II);
CAS号:15663-27-1
MDL号:MFCD00011623
EINECS号:239-733-8
RTECS号:TP2455000
PubChem号:24871609
分子式:Cl2H4N2Pt
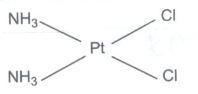
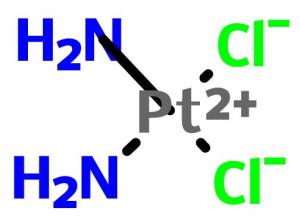 结构式:
结构式:
分子量:298.02900
精确质量:296.94000
PSA:52.04000
LogP:1.59590
物化性质
外观与性状:橙色-黄色至深黄色固体或粉末
密度:3.7
熔点:270ºC
稳定性:Stable. Incompatible with oxidizing agents, aluminium, antioxidants.
储存条件:Store in a cool, dry, well-ventilated area away from incompatible substances. Poison room locked. Keep containers tightly closed.
安全信息
符号:GHS05GHS06GHS08
信号词:危险
危害声明:H300; H318; H350
警示性声明:P201; P264; P280; P301 + P310; P305 + P351 + P338; P308 + P313
包装等级:II
 顺铂危险类别:6.1(a)
顺铂危险类别:6.1(a)
海关编码:2932999099
危险品运输编码:UN 1851/3288
WGK Germany:3
危险类别码:R45; R25; R41
安全说明:S53-S26-S39-S45
RTECS号:TP2455000
危险品标志:T[1]
计算化学数据
1、疏水参数计算参考值(XlogP):
2、氢键供体数量:2
3、氢键受体数量:4
4、可旋转化学键数量:0
5、互变异构体数量:
6、拓扑分子极性表面积(TPSA):2
7、重原子数量:5
8、表面电荷:0
9、复杂度:0
10、同位素原子数量:0
11、确定原子立构中心数量:0
12、不确定原子立构中心数量:0
13、确定化学键立构中心数量:0
14、不确定化学键立构中心数量:0
15.共价键单元数量:5
合成方法
由四氯铂酸钾与氯化铵、氨水络合制得。
用途
该品能与DNA结合,引起交叉联结,从而破坏DNA的功能,并抑制细胞有丝分裂,为一种细胞非特异性药物。该品抗瘤谱较广,用于头颈部鳞癌;卵巢癌;胚胞性癌;精原性细胞瘤;肺癌;甲状腺癌;淋巴肉瘤及网状细胞肉瘤等。[2]
安全术语
S53Avoid exposure - obtain special instructions before use.
避免接触,使用前须获得特别指示说明。
S26In case of contact with eyes, rinse immediately with plenty of water and seek medical advice.
不慎与眼睛接触后,请立即用大量清水冲洗并征求医生意见。
S39Wear eye / face protection.
戴护目镜或面具。
S45In case of accident or if you feel unwell, seek medical advice immediately (show the label whenever possible.)
若发生事故或感不适,立即就医(可能的话,出示其标签)。
风险术语
R45May cause cancer.
可能致癌。
R25Toxic if swallowed.
吞食有毒。
R41Risk of serious damage to the eyes.
对眼睛有严重伤害。
药典标准
来源、含量
本品为(Z)-二氨二氯铂。按干燥品计算,含Cl2H6N2Pt应为98.0%~102.0%。
性状
本品为亮黄色至橙黄色的结晶性粉末;无臭。本品在二甲基亚砜中易溶,在二甲基甲酰胺中略溶,在水中微溶,在乙醇中不溶。
鉴别
(1)取本品约5mg,加硫酸1ml后,即显灰绿色。
(2)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(3)取本品,加0.9%氯化钠溶液制成每1ml中约含1mg的溶液,照紫外-可见分光光度法(2010年版药典二部附录ⅣA)测定,在301nm的波长处有最大吸收,在247nm的波长处有最小吸收。
(4)本品的红外光吸收图谱应与对照的图谱(《药品红外光谱集》297图)一致。
检查
含铂量
取本品约0.5g,精密称定,照炽灼残渣检查法(2010年版药典二部附录ⅧN,但不加硫酸),在400℃炽灼至恒重,所得残渣重量即为供试量中含有铂的重量。按干燥品计算,含铂量应为64.6%~65.4%。
含氯量
取本品30mg,精密称定,照氧瓶燃烧法(2010年版药典二部附录ⅦC)进行有机破坏,用氢氧化钠试液20ml为吸收液,俟燃烧完毕后,强力振摇数分钟,用少量水冲洗瓶塞及铂丝,洗液并入吸收液中,加溴酚蓝指示液1滴,滴加稀硝酸至溶液变为黄色,再加稀硝酸1ml、乙醇20ml与1%二苯偕肼的乙醇溶液5滴,用硝酸汞滴定液(0.025mol/L)滴定,近终点时强力振摇,继续滴定至溶液显淡玫瑰红色,并将滴定的结果用空白试验校正。每1ml硝酸汞滴定液(0.025mol/L)相当于1.773mg的氯(Cl),含氯量应为23.0%~24.3%。
溶液的澄清度
取本品20mg,加0.9%氯化钠溶液20ml溶解后,溶液应澄清。
酸度
取溶液的澄清度项下的溶液,依法测定(2010年版药典二部附录ⅥH),pH值应为5.0~7.0。
有关物质
避光操作。取本品,加0.9%氯化钠溶液溶解并稀释制成每1ml中约含0.2mg的溶液,作为供试品溶液(临用新制);精密量取1ml,置50ml量瓶中,用0.9%氯化钠溶液稀释至刻度,摇匀,作为对照溶液。照含量测定项下的色谱条件,取对照溶液20μl注入液相色谱仪,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的15%。再精密量取供试品溶液和对照溶液各20μl,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的2倍。供试品溶液色谱图中如有杂质峰,相对保留时间约为0.87的杂质峰面积乘以0.569后不得大于对照溶液主峰面积的0.5倍(1.0%),相对保留时间约为1.2的杂质峰面积乘以1.356后不得大于对照溶液的主峰面积(2.0%),其他杂质峰面积的和不得大于对照溶液主峰面积的0.25(0.5%)。
干燥失重
取本品约0.1g,在105℃干燥至恒重,减失重量不得过0.5%(2010年版药典二部附录Ⅷ L)。
含量测定
照高效液相色谱法(2010年版药典二部附录ⅤD)测定。
色谱条件与系统适用性试验
用十八烷基硅烷键合硅胶为填充剂;以0.003mol/L庚烷磺酸钠的0.9%氯化钠溶液为流动相;检测波长为220nm。理论板数按顺铂峰计算不低于3000,顺铂峰与相邻杂质峰的分离度应符合要求。
测定法
避光操作。取本品适量,精密称定,加0.9%氯化钠溶液溶解并定量稀释制成每1ml中约含40μg的溶液,精密量取20μl注入液相色谱仪,记录色谱图;另取顺铂对照品,同法测定。按外标法以峰面积计算,即得。
药品说明
药理作用
顺铂又称顺氯氨铂、氯氨铂、DDP、锡铂、乙铂定、顺-双氯双氨络铂,是目前常用的金属铂类络合物,在分子中铂原子对其抗肿瘤作用有重要意义。但只有顺式才有意义,反式无效。可与DNA链交叉连接,显示出细胞毒作用。溶解后在体内无需载体转运,即可通过带电的细胞膜。由于细胞内氯离子浓度低 (4mmol/L),氯离子为水所取代,电荷呈阳性,具有类似烷化剂双功能基团的作用,可与细胞核内DNA的碱基结合,形成三种形式的交联,造成DNA损伤,破坏DNA复制和转录,高浓度时也抑制RNA及蛋白质的合成。顺铂具有抗癌谱广、乏氧细胞有效、作用性强等优点,已普遍用于治疗睾丸癌、卵巢癌、子宫癌、膀胱癌、颈部癌、前列腺癌、脑癌等,疗效显著。但顺铂用于治疗癌有一定的毒性,会引起副作用,因此需要不断寻找毒性较小而临床效果与顺铂相近的类似物。迄今各国科学家已合成并检验了数千种与顺铂相关的金属配合物,研制出以碳铂为代表的第二代抗癌铂配合物。第三代抗癌金属配合物也已发现,以二氯茂钛为代表。这些化合物从化学角度上与顺铂无关,但它们对顺铂治疗效果不大的某些癌变有较好的效果,且不伤害肾功能。现在这一领域仍在继续进行大量研究,着重在分子水平上探索金属配合物抗癌活性的机理。中国已生产商品顺铂和开展这方面的研究工作。
顺铂属于细胞周期的非特异性药物,具有细胞毒性,由于癌细胞较正常细胞的增殖和合成更为迅速,癌细胞对本品的细胞毒性作用就更为敏感,可抑制癌细胞DNA复制过程,并损伤其细胞膜上的结构,有较强的广谱抗癌作用。用于卵巢癌、前列腺癌、睾丸癌等泌尿生殖系统恶性肿瘤,有较好疗效。与长春新碱、环磷酰胺、5-氟尿嘧啶联用,对恶性淋巴瘤、乳腺癌、头颈部鳞癌、甲状腺癌成骨肉瘤等均能显效。顺铂配合放疗治疗晚期非小细胞肺癌、鼻咽癌、食管癌等疗效突出,对肝癌和软组织肉瘤也有一定疗效。顺铂为强蓄积性药物,易产生肾毒性,消化道反应较常见,部分患者出现粒细胞减少,但停药后7~14天内可恢复。
此外,本品对DNA的损伤还有可能在核内或细胞表面改变其抗原性,使原来隐蔽的表面抗原暴露,刺激抗体的免疫抑制而发挥其细胞毒作用。[3]
药动学
[体内过程] DDP口服无效,静脉注射后开始在肝、肾、大小肠及皮肤中分布最多,18~24小时后肾内积蓄最多,而脑组织中最少。在血浆中消失迅速,呈双相型。开始血浆半衰期为25~49分钟,分布后血浆半衰期为55~73小时。静脉注射后1小时血浆含量为10%左右,90%与血浆蛋白等大分子结合。排泄较慢,1日内尿中排出19%~34%,4日内尿中仅排出25%~44%,但在全剂量注入后的5日内,仅有27%~43%的顺铂排出体外;胆道或肠道排出甚少,腹腔给药时腹腔器官的药物浓度相当于静脉给药的2.5~8倍,这对卵巢癌等治疗有增效作用。[4]
适应症
小细胞与非小细胞肺癌、睾丸癌、卵巢癌、宫颈癌、子宫内膜癌、前列腺癌、膀胱癌、黑色素瘤、肉瘤、头颈部肿瘤及各种鳞状上皮癌和恶性淋巴瘤的治疗。[4]
临床应用
 肾DDP具有抗癌谱广、作用强、与多种抗肿瘤药有协同作用、且无交叉耐药等特点,为当前联合化疗中最常用的药物之一。(1) 生殖系统肿瘤:对卵巢癌及睾丸癌疗效显著。DDP与ADM的联合化疗可使40%以上的卵巢癌取得较好疗效;DDP与BLM、VLB的联合化疗,对非精原细胞睾丸癌的有效率与治愈率分别达到80%和60%。亦可用于绒癌、宫颈癌等其他生殖系统肿瘤。
肾DDP具有抗癌谱广、作用强、与多种抗肿瘤药有协同作用、且无交叉耐药等特点,为当前联合化疗中最常用的药物之一。(1) 生殖系统肿瘤:对卵巢癌及睾丸癌疗效显著。DDP与ADM的联合化疗可使40%以上的卵巢癌取得较好疗效;DDP与BLM、VLB的联合化疗,对非精原细胞睾丸癌的有效率与治愈率分别达到80%和60%。亦可用于绒癌、宫颈癌等其他生殖系统肿瘤。
(2) 头颈部癌:鼻咽癌、甲状腺癌、喉癌等。
(3) 对膀胱癌、肺癌、恶性淋巴瘤、乳腺癌、肾细胞癌、前列腺癌、软组织肉瘤、恶性黑色素瘤也有一定疗效。
(4) 其他:恶性胸腹水;与放疗并用,有放射增敏作用。
为治疗多种实体瘤的一线用药。与VP-16联合(EP方案)为治疗SCLC或NSCLC一线方案,联合MMC、IFO(IMP方案),或NVB等方案为治疗NSCLC常用方案,以DDP为主的联合化疗亦为晚期卵巢癌、骨肉瘤及神经母细胞瘤的主要治疗方案,与ADM、CTX等联用对多部位鳞状上皮癌、移行细胞癌有效,如头颈部、宫颈、食管及泌尿系肿瘤等。
“PVB”(DDP、VLB、BLM)可治疗大部分IV期非精原细胞睾丸癌,缓解率50%~80%。此外,本品为放疗增敏剂,国外广泛用于IV期不能手术的NSCLC的局部放疗,可提高疗效及改善生存期。
禁忌
对顺铂和其它含铂制剂过敏者、怀孕、哺乳期、骨髓机能减退、严重肾功能损害、失水过多、水痘、带状疱疹、痛风、高尿酸血症、近期感染及因顺铂而引起的外周神经病等患者禁用。[4]
用法用量
静脉注射或静脉滴注:每次20~30mg,或20mg/m2,溶于生理盐水20~30ml中静脉注射,或溶于5%葡萄糖注射液250~500ml中静脉滴注,在第1天和第8天使用为1个周期,一般3~4周重复,可间断用药3~4个周期。
大剂量:80~120mg/m2,每3周1次,同时注意水化,使患者尿量保持在2000~3000ml,也可加用甘露醇利尿。
胸腹腔注射:胸腔7~10日1次,每次30~60mg。腹腔每次100~160mg。
动脉注射:每次20~30ml,中由插管推注,连用5日为1周期,间隔3周可重复。动脉灌注主要用于头颈部肿瘤。
不良反应
1、 肾脏毒性:单次中、大剂量用药后,偶会出现轻微、可逆的肾功能障碍,可出现微量血尿。多次高剂量和短期内重复用药,会出现不可逆的肾功能障碍,严重时肾小管坏死,导致无尿和尿毒症。
2、 消化系统:包括恶心、呕吐、食欲减低和腹泻等,反应常在给药后1~6小时内发生,最长不超过24~48小时。偶见肝功能障碍、血清转氨酶增加,停药后可恢复。
3、 造血系统:表现为白细胞和(或)血小板的减少,一般与用药剂量有关,骨髓抑制一般在3周左右达高峰,4~6周恢复。
4、 耳毒性:可出现耳鸣和高频听力减低,多为可逆性,不须特殊处理。
5、 神经毒性:多见于总量超过300mg/㎡的患者,周围神经损伤多见,表现为运动失调、肌痛、上下肢感觉异常等;少数病人可能出现大脑功能障碍,亦可出现癫痫,球后视神经炎等。
6、 过敏反应:如心率加快,血压降低、呼吸困难、面部水肿、变态性发热反应等,都可能出现。
7、 其它:
高尿酸血症:常出现腿肿胀和关节痛。
血浆电解质紊乱:低镁血症、低钙血症、肌肉痉挛。
心脏毒性:少见心率失常、心电图改变、心动过缓或过速、心功能不全等。
免疫系统:会出现免疫抑制反应。
牙龈变化:牙龈会有铂金属沉积。
患者接受动脉或静脉注射的肢体可能出现局部肿胀。疼痛、红斑及皮肤溃疡、局部静脉炎等少见。也有可能出现脱发、精子、卵子形成障碍和男性乳房女性化等现象。
继发性非淋巴细胞性白血病的出现与顺铂化疗使用有关。
血管性病变,如脑缺血、冠状动脉缺血、外周血管障碍类似Ravnaud综合征等副作用少见,但可能与顺铂使用有关。
注意事项
1、使用
 神经(1)在运用较大剂量(80~120mg/m2)时,必须同时进行水化和利尿。所谓水化疗法即水化、利快活与增加尿中氯量,以降低肾脏毒性的一种治疗方法。一般在大剂量DDP给药前先给生理盐水或葡萄糖溶解1000ml加氯释后滴注。DDP用生理盐水200ml稀释后滴注。DDP给药前,一次给20%甘露醇125ml,DDP滴完后再用125ml,以达到利尿之目的。一般每日液体总量3000~4000ml ,输液从DDP给药前6~12小时开始,持续至DDP滴完后6小时为止;有的大剂量DDP一次给药,则连续输液3日,输液中根据尿量,每次给速尿40mg静脉冲入。
神经(1)在运用较大剂量(80~120mg/m2)时,必须同时进行水化和利尿。所谓水化疗法即水化、利快活与增加尿中氯量,以降低肾脏毒性的一种治疗方法。一般在大剂量DDP给药前先给生理盐水或葡萄糖溶解1000ml加氯释后滴注。DDP用生理盐水200ml稀释后滴注。DDP给药前,一次给20%甘露醇125ml,DDP滴完后再用125ml,以达到利尿之目的。一般每日液体总量3000~4000ml ,输液从DDP给药前6~12小时开始,持续至DDP滴完后6小时为止;有的大剂量DDP一次给药,则连续输液3日,输液中根据尿量,每次给速尿40mg静脉冲入。
(2)为减轻毒副作用,用药期间尚应多饮水;用药前宜选用各类止吐药;同时备用肾上腺素、皮质激素、抗组织胺药,以便急救使用;用DDP后可肌肉注射安钠咖以巩固疗效。
(3)在用药前、中、后均应监测血、尿及肝肾功能。其停药指片为:白细胞<3.5x 109/L,血小板<75x 109/L持续性恶心,呕吐;早期肾脏毒性如尿中白细胞10、红细胞10、管型5/高倍视野以上者;血清肌酐>186~351mmol/L者;过敏反应;在用药过程中发现有肾病史、肾功能不良及患有中耳炎的患者。若血清肌酐、尿素氮、白细胞、血小板等恢复到正常水平,一般情况良好,则可重复用药。
(4)本品可减少BLM的肾排泄而增加其肺毒性;与氨基甙类抗生素合用可发生致命的肾衰,并可能加重耳的损害;抗级别织胺药、吩噻嗪类等可能会掩盖DDP的耳毒性。
(5)DDP在生理盐水中溶解较慢,可加温30℃左右振荡助溶,也可选用溶液制剂。
2、 下列患者用药特别慎重:
即往有肾病史、造血系统功能不全、听神经功能障碍、用药前曾接受其它化疗或放射治疗、及非顺铂引起的外周神经炎等。
3、 治疗前后,治疗期间和每一疗程之前,应作如下检查:肝、肾功能、全血计数、血钙以及听神经功能、神经系统功能等检查。此外,在治疗期间,每周应检查全血计数。通常需待器官功能恢复正常后,才可重复下一疗程。
4、 化疗期间与化疗后,男女病人均需严格避孕。治疗后若想怀孕,需事先进行遗传学咨询。
5、 顺铂可能影响注意力集中、驾驶和机械操作能力。
6、 本品应避免接触铝金属(如铝金属注射针器等)。
7、 在化疗期间与化疗后,病人必需饮用足够的水份。
妇女用药
本品孕妇应用可导致胎儿损害,有报道在人乳汁中检测到本品,故建议哺乳期妇女应用本品时中止授乳。孕妇禁用。
药物相互作用
(1)与秋水仙碱、丙磺舒或磺吡酮(sulfinpyrazone)合用时,由于顺铂可能提高血液中尿酸的水平,必须调节其剂量,以控制高尿酸血症与痛风。
(2)抗组胺药、酚噻嗪类药或噻吨类药(thioxanthene)与顺铂合用,可能掩盖耳毒性的症状,如耳鸣、眩晕等。
(3)顺铂诱发的肾功能损害可导致博来霉素(甚至小剂量)的毒性反应。
(4)与各种骨髓抑制剂或放射治疗同用,可增加毒性作用,用量应减少。
(5)青霉胺或其它的蝥合剂、会减弱顺铂的活性。故本品不应与蝥合剂同时应用。
(6)与异环磷酰胺合用,会加重蛋白尿,同时有可能会增加耳毒性。
(7)顺铂化疗期间,由于其它具有肾毒性或耳毒性药物(例如头孢菌素或氨基甙类)会增加顺铂的毒性,需避免合并使用。
禁用诸如速尿等利尿剂以增加尿量。
(8)病人接受顺铂化疗后至少三个月,才可接受病毒疫苗接种。
制剂规格
注射剂:10mg/支,20mg/支,30mg/支,50mg/支。
药物过量
药物剂量超过120mg/m2,其毒性增加,尤其是肾毒性、骨髓毒性。
贮藏
遮光,密闭室温保存。[4]
物质毒性
| 编号 | 毒性类型 | 测试方法 | 测试对象 | 使用剂量 | 毒性作用 |
|---|---|---|---|---|---|
| 1 | 急性毒性 | 静脉注射 | 成年男性 | 2140 ug/kg/5D-I | 1.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) |
| 2 | 急性毒性 | 静脉注射 | 人类 | 1500 ug/kg/6D-I | 1.耳毒性——视力变化 2.肾、输尿管和膀胱毒性——肾功能下降 3.血液毒性——骨髓发生变化 |
| 3 | 急性毒性 | 静脉注射 | 人类 | 500 ug/kg/13D-I | 1.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) 2.肾、输尿管和膀胱毒性——肾功能下降 3.血液毒性——其他变化 |
| 4 | 急性毒性 | 静脉注射 | 人类 | 2500 ug/kg | 1.行为毒性——出现幻觉,感知扭曲 2.胃肠道毒性——恶心、呕吐 3.肾、输尿管和膀胱毒性——肾功能下降 |
| 5 | 急性毒性 | 静脉注射 | 人类 | 72 mg/kg/25D-I | 1.胃肠道毒性——恶心、呕吐 |
| 6 | 急性毒性 | Intradermal | 人类 | 40 ng/kg | 1.皮肤和附件毒性——对皮肤有刺激性 (局部暴露后) 2.皮肤和附件毒性——皮肤腐蚀 (局部暴露后) |
| 7 | 急性毒性 | 肠外 | 成年男性 | 2140 ug/kg/5D-I | 1.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) |
| 8 | 急性毒性 | 未报告 | 儿童 | 19200 ug/kg/12W-I | 1.耳毒性——视力变化 |
| 9 | 急性毒性 | 口服 | 大鼠 | 25800 ug/kg | 1.行为毒性——运动行为发生变化(具体情况具体分析) 2.胃肠道毒性——运动过度、腹泻 3.血液毒性——正细胞性贫血 |
| 10 | 急性毒性 | 腹腔注射 | 大鼠 | 6400 ug/kg | 详细作用没有报告除致死剂量以外的其他值 |
| 11 | 急性毒性 | 皮下注射 | 大鼠 | 8100 ug/kg | 1.肺部、胸部或者呼吸毒性——紫绀 2.胃肠道毒性——运动过度、腹泻 3.肾、输尿管和膀胱毒性——尿量增加 |
| 12 | 急性毒性 | 静脉注射 | 大鼠 | 8 mg/kg | 1.肾、输尿管和膀胱毒性——其他变化 |
| 13 | 急性毒性 | 肌肉注射 | 大鼠 | 9200 ug/kg | 1.行为毒性——运动行为发生变化(具体情况具体分析) 2.胃肠道毒性——运动过度、腹泻 3.血液毒性——正细胞性贫血 |
| 14 | 急性毒性 | 未报告 | 大鼠 | >5 mg/kg | 1.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) |
| 15 | 急性毒性 | 口服 | 小鼠 | 32700 ug/kg | 1.肺部、胸部或者呼吸毒性——紫绀 2.胃肠道毒性——运动过度、腹泻 3.肾、输尿管和膀胱毒性——尿量增加 |
| 16 | 急性毒性 | 腹腔注射 | 小鼠 | 6600 ug/kg | 详细作用没有报告除致死剂量以外的其他值 |
| 17 | 急性毒性 | 皮下注射 | 小鼠 | 13 mg/kg | 详细作用没有报告除致死剂量以外的其他值 |
| 18 | 急性毒性 | 静脉注射 | 小鼠 | 11 mg/kg | 详细作用没有报告除致死剂量以外的其他值 |
| 19 | 急性毒性 | 肌肉注射 | 小鼠 | 17900 ug/kg | 1.行为毒性——运动行为发生变化(具体情况具体分析) 2.胃肠道毒性——运动过度、腹泻 3.血液毒性——正细胞性贫血 |
| 20 | 急性毒性 | 肠外 | 小鼠 | 22 mg/kg | 详细作用没有报告除致死剂量以外的其他值 |
| 21 | 急性毒性 | 未报告 | 小鼠 | 10900 ug/kg | 详细作用没有报告除致死剂量以外的其他值 |
| 22 | 急性毒性 | 静脉注射 | 狗 | 2500 ug/kg | 1.胃肠道毒性——其他变化 2.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) 3.血液毒性——出现高铁血红蛋白、碳氧血红蛋白 |
| 23 | 急性毒性 | 静脉注射 | 猴 | 250 ug/kg | 详细作用没有报告除致死剂量以外的其他值 |
| 24 | 急性毒性 | 腹腔注射 | 豚鼠 | 9700 ug/kg | 1.耳毒性——视力变化 |
| 25 | 急性毒性 | 肠外 | 青蛙 | 17 mg/kg | 1.行为毒性——惊厥或癫痫发作阈值受到影响 2.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) |
| 26 | 急性毒性 | 静脉注射 | 哺乳动物 | 8 mg/kg | 1.胃肠道毒性——恶心、呕吐 |
| 27 | 慢性毒性 | 腹腔注射 | 大鼠 | 24 mg/kg/3D-I | 1.肝毒性——其他变化 2.肾、输尿管和膀胱毒性——其他变化 3.营养和代谢系统毒性——金属离子浓度发生变化 |
| 28 | 慢性毒性 | 腹腔注射 | 大鼠 | 9 mg/kg/5D-I | 1.胃肠道毒性——其他变化 2.生化毒性——抑制或诱导其他酶 |
| 29 | 慢性毒性 | 腹腔注射 | 大鼠 | 22680 ug/kg/35D-C | 1.肾、输尿管和膀胱毒性——膀胱重量发生变化 2.内分泌毒性——胸腺重量变化 3.血液毒性——正细胞性贫血 |
| 30 | 慢性毒性 | 腹腔注射 | 大鼠 | 23296 ug/kg/26W-C | 1.肝毒性——肝重量发生变化 2.肾、输尿管和膀胱毒性——尿中成分发生变化 3.内分泌毒性——胸腺重量变化 |
| 31 | 慢性毒性 | 腹腔注射 | 大鼠 | 14 mg/kg/7D-I | 1.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) 2.营养和代谢系统毒性——体重下降或体重增加速率下降 3.慢性病相关毒性——死亡 |
| 32 | 慢性毒性 | 腹腔注射 | 大鼠 | 18 mg/kg/5W-I | 1.周围神经毒性——神经或神经鞘结构发生变化 2.慢性病相关毒性——死亡 |
| 33 | 慢性毒性 | 静脉注射 | 大鼠 | 16200 ug/kg/26W-I | 1.心脏毒性——其他变化 2.肾、输尿管和膀胱毒性——其他变化 3.内分泌毒性——其他变化 |
| 34 | 慢性毒性 | 腹腔注射 | 大鼠 | 18 mg/kg/9W-I | 1.周围神经毒性——神经或神经鞘结构发生变化 |
| 35 | 慢性毒性 | 腹腔注射 | 大鼠 | 22800 ug/kg/6W-I | 1.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) 2.血液毒性——骨髓发生变化 3.骨骼肌毒性——其他变化 |
| 36 | 慢性毒性 | 静脉注射 | 大鼠 | 22 mg/kg/4W-I | 1.血液毒性——血清成分发生变化 (如TP、胆红素、胆固醇) 2.血液毒性——白细胞计数发生变化 3.血液毒性——血小板计数发生变化 |
| 37 | 慢性毒性 | 静脉注射 | 大鼠 | 18 mg/kg/20D-I | 1.肾、输尿管和膀胱毒性——其他变化 2.血液毒性——血清成分发生变化 (如TP、胆红素、胆固醇) 3.生化毒性——抑制或诱导过氧化氢酶 |
| 38 | 慢性毒性 | 腹腔注射 | 小鼠 | 40 mg/kg/8W-I | 1.周围神经毒性——三叉神经感官发生变化 2.营养和代谢系统毒性——体重下降或体重增加速率下降 3.慢性病相关毒性——死亡 |
| 39 | 慢性毒性 | 静脉注射 | 小鼠 | 11 mg/kg/5D-I | 1.大脑毒性——脑重量发生变化 2.肾、输尿管和膀胱毒性——膀胱重量发生变化 3.营养和代谢系统毒性——体重下降或体重增加速率下降 |
| 40 | 慢性毒性 | 静脉注射 | 狗 | 10500 ug/kg/90D | 1.血液毒性——血小板减少 2.营养和代谢系统毒性——体重下降或体重增加速率下降 3.生化毒性——抑制或诱导磷酸酶 |
| 41 | 慢性毒性 | 静脉注射 | 狗 | 10800 ug/kg/26W-I | 1.肾、输尿管和膀胱毒性——膀胱重量发生变化 2.血液毒性——血小板计数发生变化 3.慢性病相关毒性——睾丸重量发生变化 |
| 42 | 慢性毒性 | 静脉注射 | 狗 | 3750 ug/kg/5D-I | 1.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) 2.血液毒性——骨髓发生变化 3.慢性病相关毒性——死亡 |
| 43 | 慢性毒性 | 静脉注射 | 猴 | 12500 ug/kg/5D-I | 1.胃肠道毒性——其他变化 2.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) 3.血液毒性——骨髓发生变化 |
| 44 | 慢性毒性 | 静脉注射 | 猴 | 12500 ug/kg/12W-I | 1.周围神经毒性——神经或神经鞘结构发生变化 2.胃肠道毒性——恶心、呕吐 3.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) |
| 45 | 慢性毒性 | 腹腔注射 | 豚鼠 | 7500 ug/kg/15D-I | 1.耳毒性——视力变化 2.耳毒性——耳蜗结构或功能发生变化 3.慢性病相关毒性——死亡 |
| 46 | 慢性毒性 | 腹腔注射 | 豚鼠 | 18 mg/kg/9D-I | 1.血液毒性——血清成分发生变化 (如TP、胆红素、胆固醇) 2.营养和代谢系统毒性——体重下降或体重增加速率下降 3.慢性病相关毒性——死亡 |
| 47 | 慢性毒性 | 腹腔注射 | 豚鼠 | 15 mg/kg/30D-I | 1.耳毒性——耳蜗结构或功能发生变化 |
| 48 | 突变毒性 | 鼠伤寒沙门氏菌 | 250 ng/plate | ||
| 49 | 突变毒性 | 鼠伤寒沙门氏菌 | 300 ng/plate | ||
| 50 | 突变毒性 | 鼠伤寒沙门氏菌 | 1 nmol/plate | ||
| 51 | 突变毒性 | 鼠伤寒沙门氏菌 | 10 mg/L/20H (持续) | ||
| 52 | 突变毒性 | 大肠埃希氏菌 | 25 ug/plate | ||
| 53 | 突变毒性 | 大肠埃希氏菌 | 3 mg/L | ||
| 54 | 突变毒性 | 大肠埃希氏菌 | 50 umol/L | ||
| 55 | 突变毒性 | 大肠埃希氏菌 | 125 ng/plate | ||
| 56 | 突变毒性 | 大肠埃希氏菌 | 50 umol/L | ||
| 57 | 突变毒性 | 大肠埃希氏菌 | 35 mg/L | ||
| 58 | 突变毒性 | 大肠埃希氏菌 | 26600 nmol/L | ||
| 59 | 突变毒性 | 大肠埃希氏菌 | 250 umol/L | ||
| 60 | 突变毒性 | 大肠埃希氏菌 | 1 ug/plate | ||
| 61 | 突变毒性 | 枯草芽孢杆菌 | 15 umol/L/3H (持续) | ||
| 62 | 突变毒性 | 枯草芽孢杆菌 | 1 ug/plate | ||
| 63 | 突变毒性 | 微生物 | 250 mg/L | ||
| 64 | 突变毒性 | 微生物 | 1 mmol/L | ||
| 65 | 突变毒性 | 微生物 | 60 nmol/L | ||
| 66 | 突变毒性 | 微生物 | 1 mmol/L | ||
| 67 | 突变毒性 | 口服 | 果蝇 | 10 umol/L | |
| 68 | 突变毒性 | 肠外 | 果蝇 | 200 umol/L | |
| 69 | 突变毒性 | 肠外 | 果蝇 | 830 umol/L | |
| 70 | 突变毒性 | 口服 | 果蝇 | 40 ppm | |
| 71 | 突变毒性 | 肠外 | 果蝇 | 200 umol/L | |
| 72 | 突变毒性 | 粗糙脉孢菌 | 200 umol/L | ||
| 73 | 突变毒性 | 酿酒酵母 | 50 mg/L | ||
| 74 | 突变毒性 | 酿酒酵母 | 50 mg/L | ||
| 75 | 突变毒性 | 鲑鱼精子 | 10 mg/L | ||
| 76 | 突变毒性 | 人类淋巴细胞 | 8250 nmol/L | ||
| 77 | 突变毒性 | 人类白细胞 | 500 ug/L | ||
| 78 | 突变毒性 | 人类成纤维细胞 | 5 umol/L | ||
| 79 | 突变毒性 | 人类白细胞 | 100 umol/L | ||
| 80 | 突变毒性 | 人类卵巢 | 20 umol/L | ||
| 81 | 突变毒性 | 人类 细胞 | 10 umol/L | ||
| 82 | 突变毒性 | 人类卵巢 | 40 umol/L | ||
| 83 | 突变毒性 | 人类卵巢 | 10 umol/L | ||
| 84 | 突变毒性 | 人类 细胞 | 5 mg/L | ||
| 85 | 突变毒性 | 人类成纤维细胞 | 20 umol/L | ||
| 86 | 突变毒性 | 人类 细胞 | 10 umol/L | ||
| 87 | 突变毒性 | 人类 细胞 | 45 umol/L | ||
| 88 | 突变毒性 | 人类淋巴细胞 | 12 umol/L | ||
| 89 | 突变毒性 | 海拉细胞 | 5 umol/L | ||
| 90 | 突变毒性 | 海拉细胞 | 5 umol/L | ||
| 91 | 突变毒性 | 人类非 | 10 umol/L | ||
| 92 | 突变毒性 | 人类 细胞 | 10 umol/L | ||
| 93 | 突变毒性 | 人类 细胞 | 10 umol/L | ||
| 94 | 突变毒性 | 人类 细胞 | 10 umol/L | ||
| 95 | 突变毒性 | 人类成纤维细胞 | 10 umol/L | ||
| 96 | 突变毒性 | 海拉细胞 | 500 nmol/L | ||
| 97 | 突变毒性 | 人类淋巴细胞 | 10 mg/L | ||
| 98 | 突变毒性 | 人类 细胞 | 5 umol/L | ||
| 99 | 突变毒性 | 人类 细胞 | 5 umol/L | ||
| 100 | 突变毒性 | 人类淋巴细胞 | 8250 nmol/L | ||
| 101 | 突变毒性 | 人类卵巢 | 5 umol/L | ||
| 102 | 突变毒性 | 人类 细胞 | 20 umol/L | ||
| 103 | 突变毒性 | 人类鼠伤寒沙门氏菌 | 24 mg/kg | ||
| 104 | 突变毒性 | 人类 细胞 | 10 umol/L | ||
| 105 | 突变毒性 | 人类淋巴细胞 | 1 mg/L/24H | ||
| 106 | 突变毒性 | 人类 细胞 | 50 mg/L | ||
| 107 | 突变毒性 | 人类 细胞 | 3300 nmol/L | ||
| 108 | 突变毒性 | 人类淋巴细胞 | 250 ng/L/96H | ||
| 109 | 突变毒性 | 腹腔注射 | 大鼠 | 3500 ug/kg | |
| 110 | 突变毒性 | 大鼠 细胞 | 10 umol/L | ||
| 111 | 突变毒性 | 静脉注射 | 大鼠 | 8 mg/kg | |
| 112 | 突变毒性 | 腹腔注射 | 大鼠 | 5 mg/kg | |
| 113 | 突变毒性 | 腹腔注射 | 大鼠 | 4 mg/kg | |
| 114 | 突变毒性 | 静脉注射 | 大鼠 | 8500 ug/kg | |
| 115 | 突变毒性 | 大鼠肾 | 10 umol/L | ||
| 116 | 突变毒性 | 大鼠、鼠伤寒沙门氏菌 | 40 mg/kg | ||
| 117 | 突变毒性 | 腹腔注射 | 大鼠 | 650 ug/kg/5D | |
| 118 | 突变毒性 | 大鼠 细胞 | 1 umol/L | ||
| 119 | 突变毒性 | 腹腔注射 | 小鼠 | 100 ug/kg | |
| 120 | 突变毒性 | 小鼠 细胞 | 62500 ng/L | ||
| 121 | 突变毒性 | 腹腔注射 | 小鼠 | 10 mg/kg | |
| 122 | 突变毒性 | 小鼠白细胞 | 4 mg/L | ||
| 123 | 突变毒性 | 静脉注射 | 小鼠 | 20 mg/kg | |
| 124 | 突变毒性 | 小鼠 细胞 | 1 mg/L | ||
| 125 | 突变毒性 | 小鼠 细胞 | 1 mg/L | ||
| 126 | 突变毒性 | 小鼠乳腺 | 5 mg/L | ||
| 127 | 突变毒性 | 小鼠腹水瘤细胞 | 100 umol/L | ||
| 128 | 突变毒性 | 小鼠腹水瘤细胞 | 100 umol/L | ||
| 129 | 突变毒性 | 小鼠淋巴细胞 | 50 mg/L | ||
| 130 | 突变毒性 | 小鼠白细胞 | 1 mg/L | ||
| 131 | 突变毒性 | 小鼠 细胞 | 500 ug/L | ||
| 132 | 突变毒性 | 腹腔注射 | 小鼠 | 12 mg/kg | |
| 133 | 突变毒性 | 小鼠鼠伤寒沙门氏菌 | 2500 ug/kg | ||
| 134 | 突变毒性 | 腹腔注射 | 小鼠 | 500 ug/kg | |
| 135 | 突变毒性 | 小鼠 细胞 | 8 mg/kg | ||
| 136 | 突变毒性 | 小鼠白细胞 | 5 mg/L | ||
| 137 | 突变毒性 | 小鼠 细胞 | 2 mg/L | ||
| 138 | 突变毒性 | 静脉注射 | 小鼠 | 1300 ug/kg | |
| 139 | 突变毒性 | 小鼠 细胞 | 4 umol/L | ||
| 140 | 突变毒性 | 小鼠胚胎 | 100 nmol/L | ||
| 141 | 突变毒性 | 腹腔注射 | 小鼠 | 2500 ug/kg | |
| 142 | 突变毒性 | 小鼠大肠埃希氏菌 | 10 mg/L | ||
| 143 | 突变毒性 | 小鼠腹水瘤细胞 | 18200 ug/kg | ||
| 144 | 突变毒性 | 腹腔注射 | 小鼠 | 10 mg/kg | |
| 145 | 突变毒性 | 静脉注射 | 小鼠 | 10 mg/kg | |
| 146 | 突变毒性 | 腹腔注射 | 仓鼠 | 1 mg/kg | |
| 147 | 突变毒性 | 仓鼠肺 | 680 nmol/L | ||
| 148 | 突变毒性 | 仓鼠卵巢 | 5 mg/L | ||
| 149 | 突变毒性 | 仓鼠肾 | 1 umol/L | ||
| 150 | 突变毒性 | 仓鼠胚胎 | 100 nmol/L | ||
| 151 | 突变毒性 | 仓鼠卵巢 | 50 umol/L | ||
| 152 | 突变毒性 | 仓鼠肺 | 11 umol/L/2H | ||
| 153 | 突变毒性 | 仓鼠卵巢 | 1 umol/L | ||
| 154 | 突变毒性 | 仓鼠 细胞 | 1 mmol/L | ||
| 155 | 突变毒性 | 仓鼠肺 | 30 umol/L | ||
| 156 | 突变毒性 | 仓鼠卵巢 | 5 mg/L | ||
| 157 | 突变毒性 | 仓鼠卵巢 | 5 mg/L | ||
| 158 | 突变毒性 | 仓鼠肺 | 680 nmol/L | ||
| 159 | 突变毒性 | 仓鼠卵巢 | 5 mg/L | ||
| 160 | 突变毒性 | 仓鼠 细胞 | 330 nmol/L | ||
| 161 | 突变毒性 | 仓鼠肺 | 1 ng/L/2H | ||
| 162 | 突变毒性 | 仓鼠胚胎 | 100 nmol/L | ||
| 163 | 突变毒性 | 仓鼠卵巢 | 200 ug/L | ||
| 164 | 突变毒性 | 腹腔注射 | 仓鼠 | 10 mg/kg | |
| 165 | 突变毒性 | 仓鼠卵巢 | 1 umol/L | ||
| 166 | 突变毒性 | 仓鼠肺 | 2 mg/L/2H | ||
| 167 | 突变毒性 | 哺乳动物淋巴细胞 | 100 umol/L | ||
| 168 | 突变毒性 | 兔肾 | 5 mg/L/24H | ||
| 169 | 突变毒性 | 兔肾 | 5 mg/L/24H | ||
| 170 | 突变毒性 | 静脉注射 | 兔 | 1250 ug/kg | |
| 171 | 突变毒性 | 兔淋巴细胞 | 100 ug/L | ||
| 172 | 致癌性 | 腹腔注射 | 小鼠 | 7500 ug/kg | 1.致癌性——肿瘤(根据RTECS标准) 2.皮肤和附件毒性——肿瘤 3.生殖毒性——胎盘肿瘤 |
| 173 | 致癌性 | 腹腔注射 | 小鼠 | 16 mg/kg/19W-I | 1.致癌性——致癌(根据RTECS标准) 2.肺部、胸部或者呼吸毒性——肿瘤 |
| 174 | 致癌性 | 腹腔注射 | 小鼠 | 16204 ug/kg/10W-I | 1.致癌性——肿瘤(根据RTECS标准) 2.肺部、胸部或者呼吸毒性——肿瘤 |
| 175 | 致癌性 | 腹腔注射 | 小鼠 | 32408 ug/kg/10W-I | 1.致癌性——肿瘤(根据RTECS标准) 2.肺部、胸部或者呼吸毒性——肿瘤 |
| 176 | 生殖毒性 | 腹腔注射 | 大鼠 | 4500 ug/kg,雌性受孕 17-22 天后 | 1.生殖毒性——影响新生儿活力指数(如在出生第4天还活着) |
| 177 | 生殖毒性 | 腹腔注射 | 大鼠 | 2750 ug/kg,雌性受孕 7-11 天后 | 1.生殖毒性——产生额外的胚胎结构 (如胎盘、脐带) 2.生殖毒性——胎儿毒性(如胎儿发育不良,但不至死亡) 3.生殖毒性——影响新生儿活产指数 |
| 178 | 生殖毒性 | 腹腔注射 | 大鼠 | 9 mg/kg,雄性配种 3 天前 | 1.生殖毒性——睾丸,附睾,输精管发生变化 |
| 179 | 生殖毒性 | 腹腔注射 | 大鼠 | 300 ug/kg,雌性受孕 6 天后 | 1.生殖毒性——肌肉骨骼系统发育异常 |
| 180 | 生殖毒性 | 腹腔注射 | 大鼠 | 13 mg/kg,雌性受孕 17-22 天后 | 1.生殖毒性——影响新生儿的行为 2.生殖毒性——新生儿身体变化 |
| 181 | 生殖毒性 | 腹腔注射 | 大鼠 | 3 mg/kg,雌性受孕 3 天后 | 1.生殖毒性——植入后死亡率增加 |
| 182 | 生殖毒性 | 皮下注射 | 大鼠 | 10 mg/kg,雄性配种 5 天前 | 1.生殖毒性——雄性生精功能异常 (包括遗传物质,精子形态,精子活力和计数) 2.生殖毒性——睾丸,附睾,输精管发生变化 3.生殖毒性——前列腺,精囊,考伯氏腺,附属腺体发生变化 |
| 183 | 生殖毒性 | 皮下注射 | 大鼠 | 10 mg/kg,雄性配种 5 天前 | 1.生殖毒性——雄性生精功能异常 (包括遗传物质,精子形态,精子活力和计数) 2.生殖毒性——睾丸,附睾,输精管发生变化 3.生殖毒性——前列腺,精囊,考伯氏腺,附属腺体发生变化 |
| 184 | 生殖毒性 | 静脉注射 | 大鼠 | 4125 ug/kg,雌性受孕 7-17 天后 | 1.生殖毒性——胚胎或胎儿死亡 2.生殖毒性——新生儿死胎 3.生殖毒性——影响新生儿活力指数(如在出生第4天还活着) |
| 185 | 生殖毒性 | 静脉注射 | 大鼠 | 660 ug/kg,雌性受孕 7-17 天后 | 1.生殖毒性——产生额外的胚胎结构 (如胎盘、脐带) 2.生殖毒性——肌肉骨骼系统发育异常 3.生殖毒性——影响新生儿的行为 |
| 186 | 生殖毒性 | 静脉注射 | 大鼠 | 1650 ug/kg,雌性受孕 7-17 天后 | 1.生殖毒性——胎儿毒性(如胎儿发育不良,但不至死亡) 2.生殖毒性——其他变化 |
| 187 | 生殖毒性 | 静脉注射 | 大鼠 | 4125 ug/kg,雌性受孕 7-17 天后 | 1.生殖毒性——新生儿体重增加量减少 2.生殖毒性——新生儿身体变化 |
| 188 | 生殖毒性 | 未报告 | 大鼠 | 1 mg/kg,多代 | 1.生殖毒性——影响新生儿的行为 |
| 189 | 生殖毒性 | 口服 | 小鼠 | 8 mg/kg,雌性受孕 12 天后 | 1.生殖毒性——中枢神经系统发育异常 |
| 190 | 生殖毒性 | 腹腔注射 | 小鼠 | 8 mg/kg,雌性受孕 12 天后 | 1.生殖毒性——中枢神经系统发育异常 |
| 191 | 生殖毒性 | 腹腔注射 | 小鼠 | 3 mg/kg,雌性受孕 8 天后 | 1.生殖毒性——植入后死亡率增加 2.生殖毒性——影响产仔数 3.生殖毒性——胎儿毒性(如胎儿发育不良,但不至死亡) |
| 192 | 生殖毒性 | 腹腔注射 | 小鼠 | 1100 ug/kg,雄性配种 1 天前 | 1.生殖毒性——雄性生精功能异常 (包括遗传物质,精子形态,精子活力和计数) |
| 193 | 生殖毒性 | 腹腔注射 | 小鼠 | 20 mg/kg,雌性受孕 13 天后 | 1.生殖毒性——影响胎儿或胚胎细胞遗传物质 2.生殖毒性——中枢神经系统发育异常 |
| 194 | 生殖毒性 | 腹腔注射 | 小鼠 | 300 ug/kg,雌性受孕 8 天后 | 1.生殖毒性——胎儿毒性(如胎儿发育不良,但不至死亡) |
| 195 | 生殖毒性 | 皮下注射 | 小鼠 | 350 mg/kg,雄性配种 5 周前 | 1.生殖毒性——雄性生精功能异常 (包括遗传物质,精子形态,精子活力和计数) 2.生殖毒性——睾丸,附睾,输精管发生变化 |
| 196 | 生殖毒性 | 静脉注射 | 小鼠 | 1100 ug/kg,雄性配种 1 天前 | 1.生殖毒性——雄性生精功能异常 (包括遗传物质,精子形态,精子活力和计数) |
| 197 | 生殖毒性 | 静脉注射 | 兔 | 1625 ug/kg,雌性受孕 6-18 天后 | 1.生殖毒性——影响产仔数 2.生殖毒性——胚胎或胎儿死亡 |
可能危害
| 编号 | 毒性类型 | 测试方法 | 测试对象 | 使用剂量 | 毒性作用 |
|---|---|---|---|---|---|
| 1 | 急性毒性 | 静脉注射 | 成年男性 | 2140 ug/kg/5D-I | 1.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) |
| 2 | 急性毒性 | 静脉注射 | 人类 | 1500 ug/kg/6D-I | 1.耳毒性——视力变化 2.肾、输尿管和膀胱毒性——肾功能下降 3.血液毒性——骨髓发生变化 |
| 3 | 急性毒性 | 静脉注射 | 人类 | 500 ug/kg/13D-I | 1.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) 2.肾、输尿管和膀胱毒性——肾功能下降 3.血液毒性——其他变化 |
| 4 | 急性毒性 | 静脉注射 | 人类 | 2500 ug/kg | 1.行为毒性——出现幻觉,感知扭曲 2.胃肠道毒性——恶心、呕吐 3.肾、输尿管和膀胱毒性——肾功能下降 |
| 5 | 急性毒性 | 静脉注射 | 人类 | 72 mg/kg/25D-I | 1.胃肠道毒性——恶心、呕吐 |
| 6 | 急性毒性 | Intradermal | 人类 | 40 ng/kg | 1.皮肤和附件毒性——对皮肤有刺激性 (局部暴露后) 2.皮肤和附件毒性——皮肤腐蚀 (局部暴露后) |
| 7 | 急性毒性 | 肠外 | 成年男性 | 2140 ug/kg/5D-I | 1.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) |
| 8 | 急性毒性 | 未报告 | 儿童 | 19200 ug/kg/12W-I | 1.耳毒性——视力变化 |
| 9 | 急性毒性 | 口服 | 大鼠 | 25800 ug/kg | 1.行为毒性——运动行为发生变化(具体情况具体分析) 2.胃肠道毒性——运动过度、腹泻 3.血液毒性——正细胞性贫血 |
| 10 | 急性毒性 | 腹腔注射 | 大鼠 | 6400 ug/kg | 详细作用没有报告除致死剂量以外的其他值 |
| 11 | 急性毒性 | 皮下注射 | 大鼠 | 8100 ug/kg | 1.肺部、胸部或者呼吸毒性——紫绀 2.胃肠道毒性——运动过度、腹泻 3.肾、输尿管和膀胱毒性——尿量增加 |
| 12 | 急性毒性 | 静脉注射 | 大鼠 | 8 mg/kg | 1.肾、输尿管和膀胱毒性——其他变化 |
| 13 | 急性毒性 | 肌肉注射 | 大鼠 | 9200 ug/kg | 1.行为毒性——运动行为发生变化(具体情况具体分析) 2.胃肠道毒性——运动过度、腹泻 3.血液毒性——正细胞性贫血 |
| 14 | 急性毒性 | 未报告 | 大鼠 | >5 mg/kg | 1.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) |
| 15 | 急性毒性 | 口服 | 小鼠 | 32700 ug/kg | 1.肺部、胸部或者呼吸毒性——紫绀 2.胃肠道毒性——运动过度、腹泻 3.肾、输尿管和膀胱毒性——尿量增加 |
| 16 | 急性毒性 | 腹腔注射 | 小鼠 | 6600 ug/kg | 详细作用没有报告除致死剂量以外的其他值 |
| 17 | 急性毒性 | 皮下注射 | 小鼠 | 13 mg/kg | 详细作用没有报告除致死剂量以外的其他值 |
| 18 | 急性毒性 | 静脉注射 | 小鼠 | 11 mg/kg | 详细作用没有报告除致死剂量以外的其他值 |
| 19 | 急性毒性 | 肌肉注射 | 小鼠 | 17900 ug/kg | 1.行为毒性——运动行为发生变化(具体情况具体分析) 2.胃肠道毒性——运动过度、腹泻 3.血液毒性——正细胞性贫血 |
| 20 | 急性毒性 | 肠外 | 小鼠 | 22 mg/kg | 详细作用没有报告除致死剂量以外的其他值 |
| 21 | 急性毒性 | 未报告 | 小鼠 | 10900 ug/kg | 详细作用没有报告除致死剂量以外的其他值 |
| 22 | 急性毒性 | 静脉注射 | 狗 | 2500 ug/kg | 1.胃肠道毒性——其他变化 2.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) 3.血液毒性——出现高铁血红蛋白、碳氧血红蛋白 |
| 23 | 急性毒性 | 静脉注射 | 猴 | 250 ug/kg | 详细作用没有报告除致死剂量以外的其他值 |
| 24 | 急性毒性 | 腹腔注射 | 豚鼠 | 9700 ug/kg | 1.耳毒性——视力变化 |
| 25 | 急性毒性 | 肠外 | 青蛙 | 17 mg/kg | 1.行为毒性——惊厥或癫痫发作阈值受到影响 2.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) |
| 26 | 急性毒性 | 静脉注射 | 哺乳动物 | 8 mg/kg | 1.胃肠道毒性——恶心、呕吐 |
| 27 | 慢性毒性 | 腹腔注射 | 大鼠 | 24 mg/kg/3D-I | 1.肝毒性——其他变化 2.肾、输尿管和膀胱毒性——其他变化 3.营养和代谢系统毒性——金属离子浓度发生变化 |
| 28 | 慢性毒性 | 腹腔注射 | 大鼠 | 9 mg/kg/5D-I | 1.胃肠道毒性——其他变化 2.生化毒性——抑制或诱导其他酶 |
| 29 | 慢性毒性 | 腹腔注射 | 大鼠 | 22680 ug/kg/35D-C | 1.肾、输尿管和膀胱毒性——膀胱重量发生变化 2.内分泌毒性——胸腺重量变化 3.血液毒性——正细胞性贫血 |
| 30 | 慢性毒性 | 腹腔注射 | 大鼠 | 23296 ug/kg/26W-C | 1.肝毒性——肝重量发生变化 2.肾、输尿管和膀胱毒性——尿中成分发生变化 3.内分泌毒性——胸腺重量变化 |
| 31 | 慢性毒性 | 腹腔注射 | 大鼠 | 14 mg/kg/7D-I | 1.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) 2.营养和代谢系统毒性——体重下降或体重增加速率下降 3.慢性病相关毒性——死亡 |
| 32 | 慢性毒性 | 腹腔注射 | 大鼠 | 18 mg/kg/5W-I | 1.周围神经毒性——神经或神经鞘结构发生变化 2.慢性病相关毒性——死亡 |
| 33 | 慢性毒性 | 静脉注射 | 大鼠 | 16200 ug/kg/26W-I | 1.心脏毒性——其他变化 2.肾、输尿管和膀胱毒性——其他变化 3.内分泌毒性——其他变化 |
| 34 | 慢性毒性 | 腹腔注射 | 大鼠 | 18 mg/kg/9W-I | 1.周围神经毒性——神经或神经鞘结构发生变化 |
| 35 | 慢性毒性 | 腹腔注射 | 大鼠 | 22800 ug/kg/6W-I | 1.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) 2.血液毒性——骨髓发生变化 3.骨骼肌毒性——其他变化 |
| 36 | 慢性毒性 | 静脉注射 | 大鼠 | 22 mg/kg/4W-I | 1.血液毒性——血清成分发生变化 (如TP、胆红素、胆固醇) 2.血液毒性——白细胞计数发生变化 3.血液毒性——血小板计数发生变化 |
| 37 | 慢性毒性 | 静脉注射 | 大鼠 | 18 mg/kg/20D-I | 1.肾、输尿管和膀胱毒性——其他变化 2.血液毒性——血清成分发生变化 (如TP、胆红素、胆固醇) 3.生化毒性——抑制或诱导过氧化氢酶 |
| 38 | 慢性毒性 | 腹腔注射 | 小鼠 | 40 mg/kg/8W-I | 1.周围神经毒性——三叉神经感官发生变化 2.营养和代谢系统毒性——体重下降或体重增加速率下降 3.慢性病相关毒性——死亡 |
| 39 | 慢性毒性 | 静脉注射 | 小鼠 | 11 mg/kg/5D-I | 1.大脑毒性——脑重量发生变化 2.肾、输尿管和膀胱毒性——膀胱重量发生变化 3.营养和代谢系统毒性——体重下降或体重增加速率下降 |
| 40 | 慢性毒性 | 静脉注射 | 狗 | 10500 ug/kg/90D | 1.血液毒性——血小板减少 2.营养和代谢系统毒性——体重下降或体重增加速率下降 3.生化毒性——抑制或诱导磷酸酶 |
| 41 | 慢性毒性 | 静脉注射 | 狗 | 10800 ug/kg/26W-I | 1.肾、输尿管和膀胱毒性——膀胱重量发生变化 2.血液毒性——血小板计数发生变化 3.慢性病相关毒性——睾丸重量发生变化 |
| 42 | 慢性毒性 | 静脉注射 | 狗 | 3750 ug/kg/5D-I | 1.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) 2.血液毒性——骨髓发生变化 3.慢性病相关毒性——死亡 |
| 43 | 慢性毒性 | 静脉注射 | 猴 | 12500 ug/kg/5D-I | 1.胃肠道毒性——其他变化 2.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) 3.血液毒性——骨髓发生变化 |
| 44 | 慢性毒性 | 静脉注射 | 猴 | 12500 ug/kg/12W-I | 1.周围神经毒性——神经或神经鞘结构发生变化 2.胃肠道毒性——恶心、呕吐 3.肾、输尿管和膀胱毒性——肾小管发生变化 (包括急性肾功能衰竭,急性肾小管坏死) |
| 45 | 慢性毒性 | 腹腔注射 | 豚鼠 | 7500 ug/kg/15D-I | 1.耳毒性——视力变化 2.耳毒性——耳蜗结构或功能发生变化 3.慢性病相关毒性——死亡 |
| 46 | 慢性毒性 | 腹腔注射 | 豚鼠 | 18 mg/kg/9D-I | 1.血液毒性——血清成分发生变化 (如TP、胆红素、胆固醇) 2.营养和代谢系统毒性——体重下降或体重增加速率下降 3.慢性病相关毒性——死亡 |
| 47 | 慢性毒性 | 腹腔注射 | 豚鼠 | 15 mg/kg/30D-I | 1.耳毒性——耳蜗结构或功能发生变化 |
| 48 | 突变毒性 | 鼠伤寒沙门氏菌 | 250 ng/plate | ||
| 49 | 突变毒性 | 鼠伤寒沙门氏菌 | 300 ng/plate | ||
| 50 | 突变毒性 | 鼠伤寒沙门氏菌 | 1 nmol/plate | ||
| 51 | 突变毒性 | 鼠伤寒沙门氏菌 | 10 mg/L/20H (持续) | ||
| 52 | 突变毒性 | 大肠埃希氏菌 | 25 ug/plate | ||
| 53 | 突变毒性 | 大肠埃希氏菌 | 3 mg/L | ||
| 54 | 突变毒性 | 大肠埃希氏菌 | 50 umol/L | ||
| 55 | 突变毒性 | 大肠埃希氏菌 | 125 ng/plate | ||
| 56 | 突变毒性 | 大肠埃希氏菌 | 50 umol/L | ||
| 57 | 突变毒性 | 大肠埃希氏菌 | 35 mg/L | ||
| 58 | 突变毒性 | 大肠埃希氏菌 | 26600 nmol/L | ||
| 59 | 突变毒性 | 大肠埃希氏菌 | 250 umol/L | ||
| 60 | 突变毒性 | 大肠埃希氏菌 | 1 ug/plate | ||
| 61 | 突变毒性 | 枯草芽孢杆菌 | 15 umol/L/3H (持续) | ||
| 62 | 突变毒性 | 枯草芽孢杆菌 | 1 ug/plate | ||
| 63 | 突变毒性 | 微生物 | 250 mg/L | ||
| 64 | 突变毒性 | 微生物 | 1 mmol/L | ||
| 65 | 突变毒性 | 微生物 | 60 nmol/L | ||
| 66 | 突变毒性 | 微生物 | 1 mmol/L | ||
| 67 | 突变毒性 | 口服 | 果蝇 | 10 umol/L | |
| 68 | 突变毒性 | 肠外 | 果蝇 | 200 umol/L | |
| 69 | 突变毒性 | 肠外 | 果蝇 | 830 umol/L | |
| 70 | 突变毒性 | 口服 | 果蝇 | 40 ppm | |
| 71 | 突变毒性 | 肠外 | 果蝇 | 200 umol/L | |
| 72 | 突变毒性 | 粗糙脉孢菌 | 200 umol/L | ||
| 73 | 突变毒性 | 酿酒酵母 | 50 mg/L | ||
| 74 | 突变毒性 | 酿酒酵母 | 50 mg/L | ||
| 75 | 突变毒性 | 鲑鱼精子 | 10 mg/L | ||
| 76 | 突变毒性 | 人类淋巴细胞 | 8250 nmol/L | ||
| 77 | 突变毒性 | 人类白细胞 | 500 ug/L | ||
| 78 | 突变毒性 | 人类成纤维细胞 | 5 umol/L | ||
| 79 | 突变毒性 | 人类白细胞 | 100 umol/L | ||
| 80 | 突变毒性 | 人类卵巢 | 20 umol/L | ||
| 81 | 突变毒性 | 人类 细胞 | 10 umol/L | ||
| 82 | 突变毒性 | 人类卵巢 | 40 umol/L | ||
| 83 | 突变毒性 | 人类卵巢 | 10 umol/L | ||
| 84 | 突变毒性 | 人类 细胞 | 5 mg/L | ||
| 85 | 突变毒性 | 人类成纤维细胞 | 20 umol/L | ||
| 86 | 突变毒性 | 人类 细胞 | 10 umol/L | ||
| 87 | 突变毒性 | 人类 细胞 | 45 umol/L | ||
| 88 | 突变毒性 | 人类淋巴细胞 | 12 umol/L | ||
| 89 | 突变毒性 | 海拉细胞 | 5 umol/L | ||
| 90 | 突变毒性 | 海拉细胞 | 5 umol/L | ||
| 91 | 突变毒性 | 人类非 | 10 umol/L | ||
| 92 | 突变毒性 | 人类 细胞 | 10 umol/L | ||
| 93 | 突变毒性 | 人类 细胞 | 10 umol/L | ||
| 94 | 突变毒性 | 人类 细胞 | 10 umol/L | ||
| 95 | 突变毒性 | 人类成纤维细胞 | 10 umol/L | ||
| 96 | 突变毒性 | 海拉细胞 | 500 nmol/L | ||
| 97 | 突变毒性 | 人类淋巴细胞 | 10 mg/L | ||
| 98 | 突变毒性 | 人类 细胞 | 5 umol/L | ||
| 99 | 突变毒性 | 人类 细胞 | 5 umol/L | ||
| 100 | 突变毒性 | 人类淋巴细胞 | 8250 nmol/L | ||
| 101 | 突变毒性 | 人类卵巢 | 5 umol/L | ||
| 102 | 突变毒性 | 人类 细胞 | 20 umol/L | ||
| 103 | 突变毒性 | 人类鼠伤寒沙门氏菌 | 24 mg/kg | ||
| 104 | 突变毒性 | 人类 细胞 | 10 umol/L | ||
| 105 | 突变毒性 | 人类淋巴细胞 | 1 mg/L/24H | ||
| 106 | 突变毒性 | 人类 细胞 | 50 mg/L | ||
| 107 | 突变毒性 | 人类 细胞 | 3300 nmol/L | ||
| 108 | 突变毒性 | 人类淋巴细胞 | 250 ng/L/96H | ||
| 109 | 突变毒性 | 腹腔注射 | 大鼠 | 3500 ug/kg | |
| 110 | 突变毒性 | 大鼠 细胞 | 10 umol/L | ||
| 111 | 突变毒性 | 静脉注射 | 大鼠 | 8 mg/kg | |
| 112 | 突变毒性 | 腹腔注射 | 大鼠 | 5 mg/kg | |
| 113 | 突变毒性 | 腹腔注射 | 大鼠 | 4 mg/kg | |
| 114 | 突变毒性 | 静脉注射 | 大鼠 | 8500 ug/kg | |
| 115 | 突变毒性 | 大鼠肾 | 10 umol/L | ||
| 116 | 突变毒性 | 大鼠、鼠伤寒沙门氏菌 | 40 mg/kg | ||
| 117 | 突变毒性 | 腹腔注射 | 大鼠 | 650 ug/kg/5D | |
| 118 | 突变毒性 | 大鼠 细胞 | 1 umol/L | ||
| 119 | 突变毒性 | 腹腔注射 | 小鼠 | 100 ug/kg | |
| 120 | 突变毒性 | 小鼠 细胞 | 62500 ng/L | ||
| 121 | 突变毒性 | 腹腔注射 | 小鼠 | 10 mg/kg | |
| 122 | 突变毒性 | 小鼠白细胞 | 4 mg/L | ||
| 123 | 突变毒性 | 静脉注射 | 小鼠 | 20 mg/kg | |
| 124 | 突变毒性 | 小鼠 细胞 | 1 mg/L | ||
| 125 | 突变毒性 | 小鼠 细胞 | 1 mg/L | ||
| 126 | 突变毒性 | 小鼠乳腺 | 5 mg/L | ||
| 127 | 突变毒性 | 小鼠腹水瘤细胞 | 100 umol/L | ||
| 128 | 突变毒性 | 小鼠腹水瘤细胞 | 100 umol/L | ||
| 129 | 突变毒性 | 小鼠淋巴细胞 | 50 mg/L | ||
| 130 | 突变毒性 | 小鼠白细胞 | 1 mg/L | ||
| 131 | 突变毒性 | 小鼠 细胞 | 500 ug/L | ||
| 132 | 突变毒性 | 腹腔注射 | 小鼠 | 12 mg/kg | |
| 133 | 突变毒性 | 小鼠鼠伤寒沙门氏菌 | 2500 ug/kg | ||
| 134 | 突变毒性 | 腹腔注射 | 小鼠 | 500 ug/kg | |
| 135 | 突变毒性 | 小鼠 细胞 | 8 mg/kg | ||
| 136 | 突变毒性 | 小鼠白细胞 | 5 mg/L | ||
| 137 | 突变毒性 | 小鼠 细胞 | 2 mg/L | ||
| 138 | 突变毒性 | 静脉注射 | 小鼠 | 1300 ug/kg | |
| 139 | 突变毒性 | 小鼠 细胞 | 4 umol/L | ||
| 140 | 突变毒性 | 小鼠胚胎 | 100 nmol/L | ||
| 141 | 突变毒性 | 腹腔注射 | 小鼠 | 2500 ug/kg | |
| 142 | 突变毒性 | 小鼠大肠埃希氏菌 | 10 mg/L | ||
| 143 | 突变毒性 | 小鼠腹水瘤细胞 | 18200 ug/kg | ||
| 144 | 突变毒性 | 腹腔注射 | 小鼠 | 10 mg/kg | |
| 145 | 突变毒性 | 静脉注射 | 小鼠 | 10 mg/kg | |
| 146 | 突变毒性 | 腹腔注射 | 仓鼠 | 1 mg/kg | |
| 147 | 突变毒性 | 仓鼠肺 | 680 nmol/L | ||
| 148 | 突变毒性 | 仓鼠卵巢 | 5 mg/L | ||
| 149 | 突变毒性 | 仓鼠肾 | 1 umol/L | ||
| 150 | 突变毒性 | 仓鼠胚胎 | 100 nmol/L | ||
| 151 | 突变毒性 | 仓鼠卵巢 | 50 umol/L | ||
| 152 | 突变毒性 | 仓鼠肺 | 11 umol/L/2H | ||
| 153 | 突变毒性 | 仓鼠卵巢 | 1 umol/L | ||
| 154 | 突变毒性 | 仓鼠 细胞 | 1 mmol/L | ||
| 155 | 突变毒性 | 仓鼠肺 | 30 umol/L | ||
| 156 | 突变毒性 | 仓鼠卵巢 | 5 mg/L | ||
| 157 | 突变毒性 | 仓鼠卵巢 | 5 mg/L | ||
| 158 | 突变毒性 | 仓鼠肺 | 680 nmol/L | ||
| 159 | 突变毒性 | 仓鼠卵巢 | 5 mg/L | ||
| 160 | 突变毒性 | 仓鼠 细胞 | 330 nmol/L | ||
| 161 | 突变毒性 | 仓鼠肺 | 1 ng/L/2H | ||
| 162 | 突变毒性 | 仓鼠胚胎 | 100 nmol/L | ||
| 163 | 突变毒性 | 仓鼠卵巢 | 200 ug/L | ||
| 164 | 突变毒性 | 腹腔注射 | 仓鼠 | 10 mg/kg | |
| 165 | 突变毒性 | 仓鼠卵巢 | 1 umol/L | ||
| 166 | 突变毒性 | 仓鼠肺 | 2 mg/L/2H | ||
| 167 | 突变毒性 | 哺乳动物淋巴细胞 | 100 umol/L | ||
| 168 | 突变毒性 | 兔肾 | 5 mg/L/24H | ||
| 169 | 突变毒性 | 兔肾 | 5 mg/L/24H | ||
| 170 | 突变毒性 | 静脉注射 | 兔 | 1250 ug/kg | |
| 171 | 突变毒性 | 兔淋巴细胞 | 100 ug/L | ||
| 172 | 致癌性 | 腹腔注射 | 小鼠 | 7500 ug/kg | 1.致癌性——肿瘤(根据RTECS标准) 2.皮肤和附件毒性——肿瘤 3.生殖毒性——胎盘肿瘤 |
| 173 | 致癌性 | 腹腔注射 | 小鼠 | 16 mg/kg/19W-I | 1.致癌性——致癌(根据RTECS标准) 2.肺部、胸部或者呼吸毒性——肿瘤 |
| 174 | 致癌性 | 腹腔注射 | 小鼠 | 16204 ug/kg/10W-I | 1.致癌性——肿瘤(根据RTECS标准) 2.肺部、胸部或者呼吸毒性——肿瘤 |
| 175 | 致癌性 | 腹腔注射 | 小鼠 | 32408 ug/kg/10W-I | 1.致癌性——肿瘤(根据RTECS标准) 2.肺部、胸部或者呼吸毒性——肿瘤 |
| 176 | 生殖毒性 | 腹腔注射 | 大鼠 | 4500 ug/kg,雌性受孕 17-22 天后 | 1.生殖毒性——影响新生儿活力指数(如在出生第4天还活着) |
| 177 | 生殖毒性 | 腹腔注射 | 大鼠 | 2750 ug/kg,雌性受孕 7-11 天后 | 1.生殖毒性——产生额外的胚胎结构 (如胎盘、脐带) 2.生殖毒性——胎儿毒性(如胎儿发育不良,但不至死亡) 3.生殖毒性——影响新生儿活产指数 |
| 178 | 生殖毒性 | 腹腔注射 | 大鼠 | 9 mg/kg,雄性配种 3 天前 | 1.生殖毒性——睾丸,附睾,输精管发生变化 |
| 179 | 生殖毒性 | 腹腔注射 | 大鼠 | 300 ug/kg,雌性受孕 6 天后 | 1.生殖毒性——肌肉骨骼系统发育异常 |
| 180 | 生殖毒性 | 腹腔注射 | 大鼠 | 13 mg/kg,雌性受孕 17-22 天后 | 1.生殖毒性——影响新生儿的行为 2.生殖毒性——新生儿身体变化 |
| 181 | 生殖毒性 | 腹腔注射 | 大鼠 | 3 mg/kg,雌性受孕 3 天后 | 1.生殖毒性——植入后死亡率增加 |
| 182 | 生殖毒性 | 皮下注射 | 大鼠 | 10 mg/kg,雄性配种 5 天前 | 1.生殖毒性——雄性生精功能异常 (包括遗传物质,精子形态,精子活力和计数) 2.生殖毒性——睾丸,附睾,输精管发生变化 3.生殖毒性——前列腺,精囊,考伯氏腺,附属腺体发生变化 |
| 183 | 生殖毒性 | 皮下注射 | 大鼠 | 10 mg/kg,雄性配种 5 天前 | 1.生殖毒性——雄性生精功能异常 (包括遗传物质,精子形态,精子活力和计数) 2.生殖毒性——睾丸,附睾,输精管发生变化 3.生殖毒性——前列腺,精囊,考伯氏腺,附属腺体发生变化 |
| 184 | 生殖毒性 | 静脉注射 | 大鼠 | 4125 ug/kg,雌性受孕 7-17 天后 | 1.生殖毒性——胚胎或胎儿死亡 2.生殖毒性——新生儿死胎 3.生殖毒性——影响新生儿活力指数(如在出生第4天还活着) |
| 185 | 生殖毒性 | 静脉注射 | 大鼠 | 660 ug/kg,雌性受孕 7-17 天后 | 1.生殖毒性——产生额外的胚胎结构 (如胎盘、脐带) 2.生殖毒性——肌肉骨骼系统发育异常 3.生殖毒性——影响新生儿的行为 |
| 186 | 生殖毒性 | 静脉注射 | 大鼠 | 1650 ug/kg,雌性受孕 7-17 天后 | 1.生殖毒性——胎儿毒性(如胎儿发育不良,但不至死亡) 2.生殖毒性——其他变化 |
| 187 | 生殖毒性 | 静脉注射 | 大鼠 | 4125 ug/kg,雌性受孕 7-17 天后 | 1.生殖毒性——新生儿体重增加量减少 2.生殖毒性——新生儿身体变化 |
| 188 | 生殖毒性 | 未报告 | 大鼠 | 1 mg/kg,多代 | 1.生殖毒性——影响新生儿的行为 |
| 189 | 生殖毒性 | 口服 | 小鼠 | 8 mg/kg,雌性受孕 12 天后 | 1.生殖毒性——中枢神经系统发育异常 |
| 190 | 生殖毒性 | 腹腔注射 | 小鼠 | 8 mg/kg,雌性受孕 12 天后 | 1.生殖毒性——中枢神经系统发育异常 |
| 191 | 生殖毒性 | 腹腔注射 | 小鼠 | 3 mg/kg,雌性受孕 8 天后 | 1.生殖毒性——植入后死亡率增加 2.生殖毒性——影响产仔数 3.生殖毒性——胎儿毒性(如胎儿发育不良,但不至死亡) |
| 192 | 生殖毒性 | 腹腔注射 | 小鼠 | 1100 ug/kg,雄性配种 1 天前 | 1.生殖毒性——雄性生精功能异常 (包括遗传物质,精子形态,精子活力和计数) |
| 193 | 生殖毒性 | 腹腔注射 | 小鼠 | 20 mg/kg,雌性受孕 13 天后 | 1.生殖毒性——影响胎儿或胚胎细胞遗传物质 2.生殖毒性——中枢神经系统发育异常 |
| 194 | 生殖毒性 | 腹腔注射 | 小鼠 | 300 ug/kg,雌性受孕 8 天后 | 1.生殖毒性——胎儿毒性(如胎儿发育不良,但不至死亡) |
| 195 | 生殖毒性 | 皮下注射 | 小鼠 | 350 mg/kg,雄性配种 5 周前 | 1.生殖毒性——雄性生精功能异常 (包括遗传物质,精子形态,精子活力和计数) 2.生殖毒性——睾丸,附睾,输精管发生变化 |
| 196 | 生殖毒性 | 静脉注射 | 小鼠 | 1100 ug/kg,雄性配种 1 天前 | 1.生殖毒性——雄性生精功能异常 (包括遗传物质,精子形态,精子活力和计数) |
| 197 | 生殖毒性 | 静脉注射 | 兔 | 1625 ug/kg,雌性受孕 6-18 天后 | 1.生殖毒性——影响产仔数 2.生殖毒性——胚胎或胎儿死亡 |



 求购
求购

