- 骨不愈合

骨不愈合
概述
骨折在正常愈合所需时间内,仍未达到完全愈合的标准,称为延迟愈合,这里的"所需时间"通常为4个月;在8个月后骨折两断端未能达到骨性连接的骨折称为骨不连接(或称不愈合)。
骨折不愈合又叫骨不连,骨折所需愈合时间再三延长后,骨折仍没有愈合,断端仍有异常活动,X线片显示骨折断端互相分离,骨痂稀少,两断端萎缩光滑,骨髓腔封闭,骨端硬化者,称骨折不愈合。临床上常由于骨折端夹有较多的软组织,或开放性骨折清创中过多地去除碎骨片,造成骨缺损,多次的手术整复破坏了骨折部位的血液循环,对造成骨折迟缓愈合的因素没有及时去除,发展下去也可造成骨不愈合。
形成原因
骨折的延迟愈合和不愈合是骨科中的疑难问题之一。引起延迟愈合和不愈合的原因可分为治疗方面的和生理方面的,或者两方面的问题都有。
1、治疗方面的原因这方面的问题包括感染、复位差、过度牵引、反复粗暴地整复、在创伤或手术过程中破坏了局部血供、软组织嵌夹、使用不当的药物等。这些原因造成的愈合障碍大约占总的骨折愈合障碍的70%-80%。它们对皮质骨的影响一般比对松质骨的影响要严重。这类问题一般不需要进行骨移植来加速愈合,只需消除相应的因素如限制过度活动、抗感染、改善复位等通常都可愈合,对断端造成二次创伤可以促进愈合。技术原因造成的愈合障碍在40年代以前是骨折愈合障碍中的主要问题。由于抗生素和外科手术及内固定技术的发展,现在这类问题大都容易得到解决。
1.1 药物
某些治疗药物可引起骨折延迟愈合或不愈合。
抗凝药通常用来治疗或防止静脉血栓的形成,或预防肺栓塞,而且肺栓塞又是创伤骨折并不少见的并发症。实验证明双香豆素和肝素延迟家兔和狗的骨折愈合,预防剂量的双香豆素就可导致延迟愈合,不过这类药物的生物有效期不长。实验证明对骨折动物连续3周给予治疗剂量的双香豆素和肝素,3周后骨折部位为没成熟的骨,充满纤维结缔组织,有纤维桥形成,但是没有骨组织。但是临床和实验没有证明华法令(一种抗凝药)有相同的作用,事实上家兔骨折后用华法令3周后抗拉强度还要高于对照组,治疗用肝素导致的骨折延迟愈合是由于骨痂中的软骨成分增加,不过这种作用是暂时的。从实际出发,可以认为骨折病人并不禁忌抗凝治疗。
可的松至少在大剂量时抑制骨的形成,应用大剂量可的松因抑制生骨使骨痂软骨发生异常变化而出现延迟愈合。
消炎痛曾是治疗类风湿的首选药物,动物实验表明它严重妨碍大鼠股骨骨折的愈合,并且短期内出现假关节。因此有人建议,所有可能用于骨折病人的新药,都应该在动物中进行对骨折愈合毒性实验。近期研究表明消炎痛能抑制前列腺素的合成,可能是它妨碍骨折愈合的原因。
1.2骨折端分离
这是骨折不愈合通常见的,大都由肌肉牵拉或过度牵引所致。常见部位是大块肌肉附着的骨或骨突。由于肌肉的牵拉使骨分离,断端不能很好地对位。因此需要穿针或钢丝固定。髌骨横断骨折、鹰咀骨折、喙突骨折、大转子、小转子骨折、跟骨骨折都属于这种类型。移位的股骨头下骨折,由于缺乏骨膜骨痂,和股骨头缺血性坏死的倾向,更加重了骨不愈合的可能性。如果不用穿针牢固对位和固定,几乎总是发生不愈合。
肱骨干骨折,由于前臂和骨折远端的重力作用,使骨折部位经常处于受牵拉状态,所以也会影响愈合。胫骨干骨折由于持续牵拉作用也会发生骨折分离。胫骨干骨折即使有0.5cm的间隙,也会严重延迟愈合甚至不愈合。当然在这类骨折中由于缺少外部骨痂和严重的骨坏死也是造成延迟愈合和不愈合的危险因素。
1.3 肌肉的嵌入
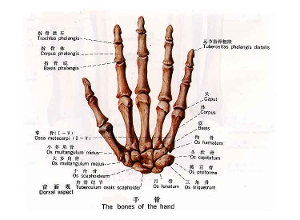 骨不愈合长骨干骨折由于嵌入肌肉或软组织造成延迟愈合或不愈合者大多是手术造成的。在大量肌肉包围的长骨干骨折这种情况并不少见。然而实验观察发现在骨折不同时期会有一些肌肉、筋膜、甚至关节软骨,有时还有肌腱和神经组织嵌在骨折断端之间。在大多数情况下,这些被嵌入的组织都会坏死、纤维化被吸收,对生骨并没有严重影响。在胫骨干骨折时这些组织会持续数周甚至数月,但是还不能断定它们是否在纤维愈合中起着某种作用。Altner将狗的尺骨造成一个窄的缺损,中间嵌入肌肉,观察对愈合的影响。5个月后,发现形成了纤维组织和软骨桥的形成并发生了坚硬的骨性愈合,与没有嵌入肌肉的对照动物没有差别。然而肌肉的嵌入不能忽视,因为它的作用可能与骨折缝的大小有关,同时嵌入肌肉的量以及它们的存活性能都会影响愈合。
骨不愈合长骨干骨折由于嵌入肌肉或软组织造成延迟愈合或不愈合者大多是手术造成的。在大量肌肉包围的长骨干骨折这种情况并不少见。然而实验观察发现在骨折不同时期会有一些肌肉、筋膜、甚至关节软骨,有时还有肌腱和神经组织嵌在骨折断端之间。在大多数情况下,这些被嵌入的组织都会坏死、纤维化被吸收,对生骨并没有严重影响。在胫骨干骨折时这些组织会持续数周甚至数月,但是还不能断定它们是否在纤维愈合中起着某种作用。Altner将狗的尺骨造成一个窄的缺损,中间嵌入肌肉,观察对愈合的影响。5个月后,发现形成了纤维组织和软骨桥的形成并发生了坚硬的骨性愈合,与没有嵌入肌肉的对照动物没有差别。然而肌肉的嵌入不能忽视,因为它的作用可能与骨折缝的大小有关,同时嵌入肌肉的量以及它们的存活性能都会影响愈合。
1.4 断端不稳定
尽管许多骨折有固有的不稳定性,在愈合过程中不断活动,还是会通过发生大量的外部骨痂固定断端,最后很好地愈合。肋骨和锁骨骨折就是很好的例子。然而胫骨干骨折如果不稳定就会造成纤维连接甚至断端分离。这时会破坏修复组织,如果再加上断端分离和缺血性坏死,更容易引起不愈合。
断端之间如果有旋转剪力,也会发生不愈合。当髓内针固定较紧完全避免旋转时,可发生暂时性骨性愈合,然而当髓内针松动时,便形成纤维连接,虽然骨膜骨痂可能很多,但断端之间是纤维桥。一些动物的纤维桥甚至出现裂隙,被一层具有绒毛的滑膜样物质包围着形成假关节。
1.5 缺血性坏死
这也是骨不连接的一个重要因素。移位的股骨头下骨折和腕骨的舟骨骨折易出现这类情况。在存活的和没存活的两断片之间会出现纤维或纤维搭桥,甚至经过很长时间之后会发生骨性替代。这种纤维连接可能是通过非特异性瘢痕组织,因为这种组织比骨性连接来得容易并发生得要快些。
在2个坏死的皮质骨之间通常会产生暂时性骨性愈合,这要靠外骨膜和内骨膜的生骨作用。骨膜骨痂或骨髓的生骨作用推迟或失败,则在皮质骨间隙之间形成纤维连接,特别是皮质坏死较严重时。
1.6化脓性感染
感染是胫骨干骨折和股骨转子间和转子下骨折用内固定时容易出现纤维性骨不愈合的主要原因。股骨上段包括头下骨折的感染,往往是由于手术伤口的感染沿着针道而扩散所致。有时附近的病灶通过败血症扩展到骨折部位引起感染,比如盆骨骨折时骶骨或臀部深处有压痛;皮肤坏死后的焦痂也可引起胫骨骨折的感染。
大多数胫骨骨折的感染都是由于开放伤口直接引起的细菌感染,或是开放复位或手术固定引起的术后感染。闭合整复的闭合骨折的感染率只有0%-0.2%,手术治疗的闭合骨折稍高一点,(1.2%-3.8%),开放骨折用保守治疗者感染率已相当高(5%-17%),手术复位或内固定者感染率为1%~17%,如用稳定的内固定,感染率在3%-7.6%之间(Karlstrom和Olerud l974年)。
在极少数情况下,胫骨或其他一些骨折可因肺部感染或其他远处开放骨折的感染由于细菌的扩散而感染。这可导致一些闭合骨折发生化脓性骨髓炎。受化脓性微生物感染的主要病理表现类似于血源性骨髓炎。
2、生理学方面的原因
骨折愈合生理方面出现障碍,即使治疗得当也不能达到正常愈合。这类问题引起的愈合障碍约占20%,另有20%合并有这类问题。
2.1 不生成骨痂或骨痂生成量少
由于生成骨痂的各种调节机制发生障碍而造成骨痂量少。这种调节机制目前还不十分清楚,包括骨痂生成的启动、致敏、刺激、增殖、分化和机化。这类问题在生理学原因造成的延迟愈合或不愈合中是主要的。长骨骨折后2个月以上X线片上没有骨痂,就表明局部生理学条件不能生成骨痂,或者整体代谢异常不能使软骨或类骨质矿化,或者两者兼有。肿瘤的放射治疗或细胞毒素(cytotoxine)治疗都可能引起这类问题,非甾类抗炎药物也可能引起这类问题。
2.2 局部加速机制异常
局部加速机制异常可引起骨痂生成缓慢、板层骨替代困难。RAP异常在长骨骨折中仅占3%,但它却占生理学问题引起的延迟愈合和不愈合的75%。
2.3 骨痂矿化障碍大多数骨软化症(但抗维生素D骨软化症除外)矿化障碍而导致假骨折和骨折、截骨术后、骨移植术后的骨不愈合。这种情况很少,大约只占全部延迟愈合和不愈合的3%。
2.4细胞分化障碍
这类病人在愈合的开始阶段,组织的激活-增殖-分化反应都正常,但是只产生成纤维细胞或脂肪母细胞而不产生成软骨细胞或(和)成骨细胞,骨折间隙充满瘢痕组织或脂肪而不是骨痂。一些转移癌和治疗不当(特别是过牵)可导致分化障碍;慢性原发性甲旁亢、神经纤维瘤、糖尿病性神经变性等通常都可引起分化障碍。
2.5 再造阶段功能障碍
以骨多细胞单位(BMU)为基础的再造机制出现原因不明的障碍,可能推迟骨痂中板层骨的替代。骨痂不能提供持久的力学结构材料。这类患者在开始时,愈合过程在骨痂的组织种类和速度方面都进行得很正常,但是在恢复功能阶段骨痂却是有塑性易变型的。这类病例十分少见。
2.6 塑造阶段障碍
主要出现在成骨不全的儿童。多发骨折造成畸形并呈现进行性加重为特点。这类病人骨痂的生成和板层骨的替代通常是正常的,塑造缺陷通常是局部的而不是全身的。如果板层骨替代编织骨全面或接近全面障碍,这类儿童出生后不久就会死亡,甚至出生前便死亡。
在骨骼成熟以后骨也会失去塑造功能,这类成年人往往在骨折1年以后,x线片显示骨外膜和皮质骨及内骨膜表面变形。
2.7 影响骨塑造的机制
使骨痂正确塑造的主要刺激因子可能不是来自骨折本身,而是来自于生物体对于仍处于柔软阶段的愈合中的骨所受的不断增长的局部牵拉力的生物学反应。因此,设想存 在一种最佳的力学范围,太大和太小的力学负重对骨折愈合都是不利的。骨骼肌的牵拉和体重都是这类力的来源,进行中的RAP机制对这些力产生反应,促使骨痂正确地塑造。
如何判断
骨折在预定愈合时间仍有疼痛、软组织肿胀,提示骨折愈合受阻。X线片示骨折端无骨痂或有很少骨痂形成,骨折线骨质疏松。如骨折处有异常活动,X线片示骨折端髓腔封闭,骨端膨张大,骨折间隙加大,临床诊断为骨折不愈合。有严重骨质疏松的患者仅有骨折端萎缩、骨折间隙加宽。这一点与骨折延期愈合很难截然分开。通过延长固定时间观察如无骨愈合迹象则按骨不连处理。这类病人虽看不到骨端硬化,但手术中看到骨折端形成致密纤维瘢痕,影响骨痂连接。
对骨折病人从治疗开始就要制定出严格的治疗计划,防止骨折愈合障碍。骨折后要立即制动,防止损伤加重。手法复位达到功能复位即可,不必为达到“完全复位”多次整复。骨折固定要可靠。要指导病人积极进行功能锻炼,促进骨折愈合。行小夹板或石膏固定时要观察肢体是否受压。有压迫时要及时解除,以免造成静脉回流受阻。手术治疗要选择损伤小,固定可靠的方法。如股骨颈骨折尽量选用多针内固定,不用三刃钉,因其对骨组织损伤过大。股骨干骨折尽量选用髓内针或钢板固定,不用安达钉,因其固定不确实。胫骨干骨折尽量不手术治疗,因加重骨折端血运及骨膜损伤,
症状及临床表现
2. 疼痛:骨端在移动时或试做负重时,产生疼痛。
3. 畸形与肌萎缩:未连接的骨折,可有成角、缩短与旋转畸形。由于长期不能使用肢体,关节挛缩畸形与肌萎缩都可出现。
4. 负重功能丧失:骨干骨折后的骨不连负重功能丧失,但某些股骨颈骨折有跛行。
5. 骨传导音降低:骨不连或延迟连接,骨传导音较健侧弱。
促进愈合
1、断端的活动
正确的复位和充足的血供是骨折愈合的必要条件。西方医学在过去曾过分强调解剖复位和坚强固定,提出"广泛固定、完全休息"是治疗骨折的指导原则。在这一原则的指导下,提出一期愈合(直接愈合)的理论,即加压钢板固定,不通过软骨骨痂阶段,直接在骨折缝产生骨性愈合。但这种愈合方式非常缓慢,内固定物在术后1-1.5年取出后,有的骨折还需要用外固定加以保护。
近代研究表明坚强固定有的需要切除和剥离骨膜,影响骨膜循环,有的破坏皮质和髓腔,同时刺激破骨细胞产生骨吸收使骨变得疏松,不利于骨折愈合。同时由于对断端的绝对固定,坚硬的内固定器材对骨折端产生应力遮挡,使骨折端"绝对休息",没有刺激,骨折端就不会向骨折间隙分泌刺激骨折愈合的因子,因此愈合过程缓慢。不同的骨骨折所需要固定的程度是不同的,肋骨在持续活动下可以愈合,而长骨却不能。但即使长骨也需要一定的功能活动。功能活动不仅是治疗骨折的目的,也是促进骨折愈合的重要手段。
作为对坚强内固定的反省,近来开始用石墨纤维和甲基丙烯酸甲酯做成的较柔软的板,这类树脂板对人类还没有作出生物适应性结论,但它们会成为理论上和实践上有用的东西,它们较低的弹性模量迫使骨去承担一部分负重压力。动物实验表明,这些材料都减少骨质疏松,增加骨的形成。
2、 生物电刺激 骨不愈合如上所述,通过相对活动骨折端产生的应力能促进骨修复。近来研究认为这种刺激的本质是"生物电"。Basser发现,皮质骨经受压力或张力时会产生1-2mV的电压,这种现象称为"压电"。这种现象只有钙化了的骨才会发生,预先脱了钙的骨就不会产生压电。
骨不愈合如上所述,通过相对活动骨折端产生的应力能促进骨修复。近来研究认为这种刺激的本质是"生物电"。Basser发现,皮质骨经受压力或张力时会产生1-2mV的电压,这种现象称为"压电"。这种现象只有钙化了的骨才会发生,预先脱了钙的骨就不会产生压电。
Rodan等认为,微小的电流对骨产生一"触发"刺激作用,或者说是提供一个启动一系列细胞现象的阈值。这些现象包括反分化、干细胞的增生和分化最终成为生骨细胞系。这一概念由下列实验依据推出:①直流电刺激鸡软骨和19d大鼠颅骨DNA的合成;②增加骨细胞中与胶原合成有关的细胞内微结构(线粒体、粗面内质网、微粒体等);③改变细胞形态;④增加碱性磷酸酶在骨细胞表面的聚集。这些作用对骨中的细胞是特异的,大鼠脾脏的成纤维细胞和淋巴细胞对直流电没有反应。而且直流电还可使生骨细胞增加cGMP和Ca2+,减少cAMP。大多数细胞的生长相总是伴随着cAMP的减少。Davidovich报道,当牙齿矫形应力刺激骨细胞重建下颌骨时,细胞中的cAMP水平便下降。这说明生物电的触发刺激还包括细胞膜双极化。
近来,临床上对应用电流治疗难愈合的骨折很感兴趣,电刺激治疗不愈合的经验已由Spadaro进行过总结。他还计算出当这些骨折愈合时,沉积到骨中的能量,大约为7J。在所有这些实验中场强似乎是决定在生骨过程中细胞的一系列过程进行得精确与否的限制因素。不难理解,在骨痂形成的不同阶段,最适宜的场强是不同的,因为骨折愈合过程中不同时期起主要作用的细胞是不同的。
3、诱导生骨上面我们提到了骨折修复过程中的一些细胞因素,如骨外膜、骨内膜和骨髓中的生骨细胞,还提到了活化这些细胞因素的内部条件,如生物电、氧分压等。骨移植已成为临床上治疗骨折愈合的重要手段。过去认为自体骨移植可以为骨折修复提供大量有活性的生骨细胞,这种看法可能过分夸大了骨移植的功能。由于移植物丧失了营养供应,在移植物表面的成骨细胞能存活的时间不长。异体移植骨的骨细胞可以存活24h,骨膜移植尽管与受体的血管建立了联系,效果也不好。所以最好的猜测是,骨移植物的主要功能是骨能存活足够长的时间,以便为宿主细胞的生长提供1个基质。所以大量的研究工作是致力于移植物的存活。冷冻、紫外线照射、灭菌、脱蛋白都是通过减少抗体蛋白来提高其生物适应性。
近20年来的研究,已经改变了"骨移植物只是被动参与骨修复"的观点。Urist积累了许多证据说明移植物含有一种生物活性物质,这种物质可以激活损伤处的居留细胞,使其在愈合中生骨。现在还不知道这种物质是否有诱导生血管的作用。这种物质叫做骨形态发生蛋白质(BMP)。现在猜测骨折后从骨折断端释放出BMP,正是BMP引起原始的没分化的细胞分化为有生骨能力的细胞。
骨中骨诱导物质的释放可能与胶原有关,BMP的活性可被骨中和牙齿中的内源性蛋白酶破坏;在不释放羟脯氨酸的情况下被胰蛋白酶降解;或被二硝基苯苯基化而破坏;BMP是碱不稳定的,其活性因酪氨酸或苯丙氨酸断裂受到抑制;通过脱氨基或巯基乙醇还原可提高活性。移植物脱钙后再抽提糖蛋白强抗原部分可强烈表现出骨诱导活性。
Oikarinen曾对比了新鲜自体骨和表面脱钙异体骨对大鼠腓骨缺损的骨诱导能力。结果,3个月后,16只用表面脱钙异体骨治疗的大鼠有15只产生了大量的骨痂,11只骨性愈合;而自体骨移植组16只中只有4只骨性愈合,12只没有愈合,有5只出现假关节。

-
锁骨下动脉盗血综合症
2025-09-20 23:48:48 查看详情


 求购
求购





