- 艾拉莫德

艾拉莫德
药品信息
中文名称:艾拉莫德
中文别名:N-[3-(甲酰胺基)-4-氧-6-苯氧基-4H-1-苯并吡喃-7-基]甲烷磺酰胺
英文名称:Iguratimod
英文别名:iguratimod( R&D); T 614; N-[7-methanesulfonamido-4-oxo-6-(phenoxy)chromen-3-yl]formamide; Ailamode; N-[3-(formylamino)-4-oxo-6-phenoxy-4H-chromen-7-yl]methanesulfonamide
外观:白色粉末
规格:企业标准含量:>99%
用途:慢作用抗风湿性药。免疫调节剂,抗风湿药。
作用机制
抗炎作用
① 艾拉莫德对急、慢性的炎症模型(如大鼠角叉菜胶足跖肿胀模型、佐剂诱导关节炎模型)均显示出抗炎、镇痛的作用。 ② 艾拉莫德不同于传统的非甾体类抗炎药物,对禁食老鼠没有表现出消化道的溃疡类不良反应。
③ 艾拉莫德能够抑制高岭土诱导的炎症反应中缓激肽
的增加。
④ 艾拉莫德在抑制花生四烯酸级联反应方面与选择性环氧酶-2(COX-2)作用形似,能有效抑制体外成纤维细胞释放前列腺素,并且减少足跖肿胀炎性反应模型鼠的炎性分泌物中PGE2的量,但不影响模型鼠的消化道粘膜中的PG水平。
抑制免疫球蛋白生成
① 小鼠B细胞培养中,艾拉莫德能够显著减少IgM的产生,并且通过脂多糖和/或IL-4的诱导向IgG1同型转换。
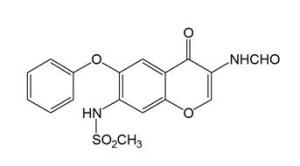 艾得辛(艾拉莫德片)分子结构式② 在人类浆细胞瘤细胞系培养中(ARH-77细胞株),艾拉莫德能抑制自发性IgG抗体生成,但并不会影响细胞增殖。③ 在由自体T细胞和抗CD3 抗体诱导的人类外周血B细胞中,艾拉莫德能够同时抑制IgM和 IgG的生成。
艾得辛(艾拉莫德片)分子结构式② 在人类浆细胞瘤细胞系培养中(ARH-77细胞株),艾拉莫德能抑制自发性IgG抗体生成,但并不会影响细胞增殖。③ 在由自体T细胞和抗CD3 抗体诱导的人类外周血B细胞中,艾拉莫德能够同时抑制IgM和 IgG的生成。
④ 艾拉莫德抑制B细胞的免疫球蛋白生成,但是不导致阻滞效应。
⑤ 在慢性类风湿实验模型(如AIA鼠和MRI/lpr鼠)中,类风湿病灶好转,同时高免疫球蛋白血症改善。
抑制细胞因子生成
艾拉莫德能够抑制IL-1β、TNFα、IL-6、IL-8以及MPC-1的生成。在由人类风湿患者体内提取的滑膜细胞中,艾拉莫德能够显著降低IL-6、IL-8以及集落刺激因子的生成。Kawakami 发现,艾拉莫德能够抑制IFN-γ刺激下的滑膜细胞中包括CD54、CD58 和CD106 等在内的联合刺激分子的上调表达。
皮下气腔炎症模型鼠口服艾拉莫德剂量为30-100mg/kg 后,静脉注射TNFα诱导的MCP-1生成被显著抑制。艾拉莫德在10-30mg/kg浓度时,除了能够降低刀豆蛋白A诱导的肝炎模型鼠的转氨酶之外,还能够减低血浆中TNFα和IFN-γ的水平。
抗骨吸收作用
IL-1、IL-6、TNF-α等促炎因子是RA致病的关键因子,与RA病情活动密切相关。这些促炎因子还能激活破骨细胞,促进骨吸收,导致骨质流失的发生。抑制IL-1、IL-6、TNF-α等促炎因子能起到控制RA及RA引起骨流失的双重效果。
在CIA大鼠模型中,MRI检测结果显示,艾拉莫德能够几乎完全抑制了CIA的炎症和骨髓内水肿;同时,X线平片和CT检测结果显示,艾拉莫德还能够显著抑制骨吸收和关节破坏。
促骨形成作用
艾拉莫德在体外试验中能促进成骨细胞分化,在体内试验中促进BMP-2介导的骨形成,该作用被认为与增加Osx的表达有关。
Osx在骨分化和骨形成中起核心作用。在骨髓基质细胞系ST2细胞中,rhBMP-2不存在时,Osx几乎不表达;rhBMP-2 存在时,艾拉莫德可刺激Osx可的表达可提高三倍以上。而在前成骨细胞系MC3T3-E1细胞中,Osx的表达不依赖于rhBMP-2,艾拉莫德能够直接刺激Osx表达而促进成骨细胞分化。
进一步研究发现,艾拉莫德能够剂量依赖性地刺激ST2细胞和MC3T3-E1细胞分泌骨钙素;在rhBMP-2存在下使ST2细胞内钙含量提高14倍,形成矿化结节;在小鼠体内模型中,使听小骨中的钙含量提高1.7倍。
临床试验
 艾拉莫德临床疗效图(14)本品Ⅰ期临床试验由南京医科大学第一附属医院国家药品临床研究基地完成,II期、III期多中心临床试验(共780例)由上海交通大学医学院附属仁济医院鲍春德教授为组长单位的协作组共同完成。
艾拉莫德临床疗效图(14)本品Ⅰ期临床试验由南京医科大学第一附属医院国家药品临床研究基地完成,II期、III期多中心临床试验(共780例)由上海交通大学医学院附属仁济医院鲍春德教授为组长单位的协作组共同完成。
I期临床试验
单次给药组的耐受性试验:完成12.5mg, 25mg, 50mg(低、中、高三个剂量组的给药试验,每组6人。多次给药组的耐受性试验:12名受试者完成25mg,每日2次×6天。
单次给药组和多次给药组各剂量组试验前后测定体温、呼吸、脉搏、心肺听诊及腹部检查、心电图均无异常;未见有临床意义的血常规、尿常规及肝肾功能异常;无血糖、血电解质的异常。各试验组均无大便潜血试验阳性。主要药动学参数在受试者的性别方面基本无明显差异。在治疗剂量范围内(25mg~50mg),艾拉莫德暴露程度与剂量呈比例。推荐Ⅱ期临床试验25mg/次,每12小时一次的给药方法或25mg/次,每24小时一次的给药方法。
II期临床试验
采用多中心、随机、双盲、安慰剂对照设计方法,评价本品的有效性和安全性,在活动性类风湿关节炎患者中比较安慰剂组、25mg组、50mg组的量效关系和安全性的差异。用法用量:25mg组:每日早晨饭后服用25mg(1片),1日1次,共24周;50mg组:每日早、晚饭后各服用25mg(1片),1日2次,共24周。在6周、12周、18周和24周进行有效性和安全性评价。有效性依据美国风湿病学会改善标准(ACR20、ACR50、ACR70),共观察了活动性类风湿关节炎患者288例,可评价病例280例,分别是安慰剂组95例,25mg组92例,50mg组93例。结果见表1。
(表1) 安慰剂组、25mg组和50mg组疗效-时间评价的比较(全分析集)
| 时间 | 疗效 | 安慰剂组(N=95) | 25mg组(N=92) | 50mg组(N=93) | P值 | |||||||
| N | % | N | % | N | % | |||||||
| 6周 | ACR20 | 13 | 13.68 | 27 | 29.35 | 32 | 34.41 | 0.0012 | ||||
| ACR50 | 1 | 1.05 | 5 | 5.43 | 8 | 8.60 | 0.0188 | |||||
| ACR70 | 0 | 0 | 1 | 1.09 | 2 | 2.15 | 0.1543 | |||||
| 12周 | ACR20 | 21 | 22.11 | 33 | 35.87 | 42 | 45.16 | 0.0008 | ||||
| ACR50 | 7 | 7.37 | 14 | 15.22 | 17 | 18.28 | 0.0314 | |||||
| ACR70 | 2 | 2.11 | 3 | 3.26 | 6 | 6.45 | 0.1387 | |||||
| 18周 | ACR20 | 27 | 28.42 | 35 | 38.04 | 55 | 59.14 | <0.0001 | ||||
| ACR50 | 8 | 8.42 | 17 | 18.48 | 23 | 24.73 | 0.0029 | |||||
| ACR70 | 2 | 2.11 | 11 | 11.96 | 10 | 10.75 | 0.0315 | |||||
| 24周 | ACR20 | 23 | 24.21 | 36 | 39.13 | 57 | 61.29 | <0.0001 | ||||
| ACR50 | 7 | 7.37 | 22 | 23.91 | 29 | 31.18 | <0.0001 | |||||
| ACR70 | 1 | 1.05 | 13 | 14.13 | 13 | 13.98 | 0.0028 | |||||
注:ACR20的反应定义是:患者疼痛及肿胀关节数(28个)有20%的改善以及下列5项中至少3项的改善:①.受试者评估的疼痛(Visual Analogue Scale/Score,简称VAS)评分;②.受试者评估的疾病总体状况VAS评分;③.研究者评估的疾病总体状况VAS评分;④.健康状况问卷(Health Assessment Questionnaire,简称HAQ);⑤.急性期反应物(血沉或C反应蛋白)。ACR50、ACR70采用相同的标准分别定义为50%及70%的改善。每项指标的改善百分数=[(治疗后值-治疗前值)/治疗前值×100%]。
试验结果表明,艾拉莫德治疗6周开始起效,安慰剂组、25mg组和50mg组疗效差异有统计学意义。25mg组疗效优于安慰剂组,50mg组疗效优于25mg组。
III期临床试验
| 时间 | 疗效 | 安慰剂组(N=95) | 25mg组(N=92) | 50mg组(N=93) | P值 | |||||||
| N | % | N | % | N | % | |||||||
| 6周 | ACR20 | 13 | 13.68 | 27 | 29.35 | 32 | 34.41 | 0.0012 | ||||
| ACR50 | 1 | 1.05 | 5 | 5.43 | 8 | 8.60 | 0.0188 | |||||
| ACR70 | 0 | 0 | 1 | 1.09 | 2 | 2.15 | 0.1543 | |||||
| 12周 | ACR20 | 21 | 22.11 | 33 | 35.87 | 42 | 45.16 | 0.0008 | ||||
| ACR50 | 7 | 7.37 | 14 | 15.22 | 17 | 18.28 | 0.0314 | |||||
| ACR70 | 2 | 2.11 | 3 | 3.26 | 6 | 6.45 | 0.1387 | |||||
| 18周 | ACR20 | 27 | 28.42 | 35 | 38.04 | 55 | 59.14 | <0.0001 | ||||
| ACR50 | 8 | 8.42 | 17 | 18.48 | 23 | 24.73 | 0.0029 | |||||
| ACR70 | 2 | 2.11 | 11 | 11.96 | 10 | 10.75 | 0.0315 | |||||
| 24周 | ACR20 | 23 | 24.21 | 36 | 39.13 | 57 | 61.29 | <0.0001 | ||||
| ACR50 | 7 | 7.37 | 22 | 23.91 | 29 | 31.18 | <0.0001 | |||||
| ACR70 | 1 | 1.05 | 13 | 14.13 | 13 | 13.98 | 0.0028 | |||||
用药方法
采用多中心、随机、双盲双模拟、阳性对照试验设计方法,评价本品的有效性和安全性,比较甲氨蝶呤组、试验组1、试验组2的量效关系和安全性的差异。受试者均为活动性类风湿关节炎患者。
用法用量:甲氨蝶呤组:第1-4周,1周1次,1次10mg(4片);第5-24周,1周1次,1次15mg(6片) ;共24周。试验组1:第1-4周:每日早晨饭后服用25mg(1片),1日1次;第5-24周:每日早、晚饭后各服用25mg(1片),1日2次;共24周。试验组2:第1-24周:每日早、晚饭后各服用25mg(1片),1日2次,共24周。在4周、10周、17周和24周进行有效性和安全性评价,有效性评价依据美国风湿病学会改善标准(ACR20、ACR50、ACR70),共观察了活动性类风湿关节炎患者492例,可评价病例489例,分别是甲氨蝶呤组:163例、试验组1:163例、试验组2:163例。试验结果见表2。
(表2)甲氨蝶呤组、试验组1、试验组2 疗效-时间评价的比较(全分析集)
| 时间 | 疗效 | 甲氨蝶呤组(N=163) | 试验组1(N=163) | 试验组2(N=163) | P值 | |||||||
| N | % | N | % | N | % | |||||||
| 4周 | ACR20 | 37 | 22.70 | 36 | 22.09 | 43 | 26.38 | 0.8801 | ||||
| ACR50 | 10 | 6.13 | 3 | 1.84 | 11 | 6.75 | 0.0659 | |||||
| ACR70 | 1 | 0.61 | 1 | 0.61 | 2 | 1.23 | 1.0000 | |||||
| 10周 | ACR20 | 87 | 53.37 | 64 | 39.26 | 77 | 47.24 | 0.0072 | ||||
| ACR50 | 27 | 16.56 | 21 | 12.88 | 30 | 18.40 | 0.3460 | |||||
| ACR70 | 11 | 6.75 | 8 | 4.91 | 14 | 8.59 | 0.4912 | |||||
| 17周 | ACR20 | 97 | 59.51 | 76 | 46.63 | 91 | 55.83 | 0.0161 | ||||
| ACR50 | 52 | 31.90 | 44 | 26.99 | 47 | 28.83 | 0.3032 | |||||
| ACR70 | 22 | 13.50 | 15 | 9.20 | 23 | 14.11 | 0.2110 | |||||
| 24周 | ACR20 | 101 | 61.96 | 83 | 50.92 | 104 | 63.80 | 0.0397 | ||||
| ACR50 | 70 | 42.94 | 53 | 32.52 | 62 | 38.04 | 0.0457 | |||||
| ACR70 | 34 | 20.86 | 27 | 16.56 | 30 | 18.40 | 0.2779 | |||||
试验结果表明:在24周终点时艾拉莫德片ACR20非劣(非劣效界值为10%)于甲氨蝶呤片。
表3显示II期、III期临床试验各单项指标的变化。
(表3) ACR反应标准各项指标的改变*
| 各项指标 | 安慰剂-对照研究 | 甲氨蝶呤-对照研究 | |||||||
| Ⅱ期临床试验(24周) | Ⅲ期临床试验(24周) | ||||||||
| 25mg组n=93 | 50mg组n=94 | 安慰剂组n=95 | 试验组1n=163 | 试验组2n=163 | 甲氨蝶呤n=165 | ||||
| 压痛关节数1 | 4.0 | 6.0 | 2.0 | 5.0 | 7.0 | 7.0 | |||
| 肿胀关节数1 | 4.5 | 6.0 | 2.0 | 4.0 | 4.0 | 5.0 | |||
| 患者总体评价2 | 18.0 | 30.0 | 5.0 | 30.0 | 28.0 | 30.0 | |||
| 医生总体评价2 | 18.5 | 31.0 | 3.0 | 27.0 | 25.0 | 30.0 | |||
| 日常生活能力(HAQ) | 0.25 | 0.40 | 0.10 | 0.40 | 0.40 | 0.45 | |||
| 疼痛程度 | 15.0 | 30.0 | 5.0 | 26.0 | 25.0 | 30.0 | |||
| 红细胞沉降率 | 3.5 | 12.0 | -4.0 | 6.0 | 8.0 | 8.0 | |||
| C反应蛋白 | 2.09 | 1.81 | 0.00 | 1.04 | 0.86 | 1.97 | |||
| 以下为ACR反应指数未包括的指标 | |||||||||
| 晨僵(min) | 60.0 | 60.0 | 30.0 | 60.0 | 60.0 | 60.0 | |||
| IgA | _ | _ | _ | 0.42 | 0.54 | 0.23 | |||
| IgG | _ | _ | _ | 0.76 | 1.30 | 0.55 | |||
| IgM | _ | _ | _ | 0.31 | 0.32 | 0.24 | |||
*末次观察值结转(LOCF):正值表明改善
1.基于28个关节数
2.直观类比标尺0=最佳,100=最坏
安全性
| 时间 | 疗效 | 甲氨蝶呤组(N=163) | 试验组1(N=163) | 试验组2(N=163) | P值 | |||||||
| N | % | N | % | N | % | |||||||
| 4周 | ACR20 | 37 | 22.70 | 36 | 22.09 | 43 | 26.38 | 0.8801 | ||||
| ACR50 | 10 | 6.13 | 3 | 1.84 | 11 | 6.75 | 0.0659 | |||||
| ACR70 | 1 | 0.61 | 1 | 0.61 | 2 | 1.23 | 1.0000 | |||||
| 10周 | ACR20 | 87 | 53.37 | 64 | 39.26 | 77 | 47.24 | 0.0072 | ||||
| ACR50 | 27 | 16.56 | 21 | 12.88 | 30 | 18.40 | 0.3460 | |||||
| ACR70 | 11 | 6.75 | 8 | 4.91 | 14 | 8.59 | 0.4912 | |||||
| 17周 | ACR20 | 97 | 59.51 | 76 | 46.63 | 91 | 55.83 | 0.0161 | ||||
| ACR50 | 52 | 31.90 | 44 | 26.99 | 47 | 28.83 | 0.3032 | |||||
| ACR70 | 22 | 13.50 | 15 | 9.20 | 23 | 14.11 | 0.2110 | |||||
| 24周 | ACR20 | 101 | 61.96 | 83 | 50.92 | 104 | 63.80 | 0.0397 | ||||
| ACR50 | 70 | 42.94 | 53 | 32.52 | 62 | 38.04 | 0.0457 | |||||
| ACR70 | 34 | 20.86 | 27 | 16.56 | 30 | 18.40 | 0.2779 | |||||
注意事项
| 各项指标 | 安慰剂-对照研究 | 甲氨蝶呤-对照研究 | |||||||
| Ⅱ期临床试验(24周) | Ⅲ期临床试验(24周) | ||||||||
| 25mg组n=93 | 50mg组n=94 | 安慰剂组n=95 | 试验组1n=163 | 试验组2n=163 | 甲氨蝶呤n=165 | ||||
| 压痛关节数1 | 4.0 | 6.0 | 2.0 | 5.0 | 7.0 | 7.0 | |||
| 肿胀关节数1 | 4.5 | 6.0 | 2.0 | 4.0 | 4.0 | 5.0 | |||
| 患者总体评价2 | 18.0 | 30.0 | 5.0 | 30.0 | 28.0 | 30.0 | |||
| 医生总体评价2 | 18.5 | 31.0 | 3.0 | 27.0 | 25.0 | 30.0 | |||
| 日常生活能力(HAQ) | 0.25 | 0.40 | 0.10 | 0.40 | 0.40 | 0.45 | |||
| 疼痛程度 | 15.0 | 30.0 | 5.0 | 26.0 | 25.0 | 30.0 | |||
| 红细胞沉降率 | 3.5 | 12.0 | -4.0 | 6.0 | 8.0 | 8.0 | |||
| C反应蛋白 | 2.09 | 1.81 | 0.00 | 1.04 | 0.86 | 1.97 | |||
| 以下为ACR反应指数未包括的指标 | |||||||||
| 晨僵(min) | 60.0 | 60.0 | 30.0 | 60.0 | 60.0 | 60.0 | |||
| IgA | _ | _ | _ | 0.42 | 0.54 | 0.23 | |||
| IgG | _ | _ | _ | 0.76 | 1.30 | 0.55 | |||
| IgM | _ | _ | _ | 0.31 | 0.32 | 0.24 | |||
词条图册
口服。一次25mg (1片),饭后服用,一日2次,早、晚各1次。



 求购
求购










